názor CNRS na práce Jacques Benveniste
Šest měsíců po jeho smrti názor CNRS na práce J. Benveniste
- března 2005
Úvod:



**
[Audiozáznam interview Montagniera, květen 2010](../../AUDIOS/LE SEPT NEUF DU DIMANCHE 02.05.2010_benveniste.mp3)
- května 2010.
Čtenář mi odeslal úryvek z pořadu, ve kterém slyším Nobelovce Luc Montagniera, který chválí mého smutného přítele Jacques Benveniste.
Profesor Luc Montagnier, Nobelovce v medicíně, 2007 v Luganu, ten se nezdržuje a bez váhání prohlašuje, že Jacques byl geniální předtečník, o krok vpřed ve své době, a jeho přesvědčení, že jednou bude uznána správnost jeho názorů.
Pamatujeme na dobu, kdy generální ředitel INSERM, Lazare, odstranil Jacquesovi jeho 200 m² pracoviště v INSERM 200 v Clamartu, což ho donutilo přesunout se do Algeco výběhu! Absolutní hanba.
Mnohokrát jsem Jacquesovi říkal: "Vzdávej, ztratíš život!" Ale držel se, držel se až do posledního dechu, až mu to stálo život, s rozbitým srdcem.
Moje kariéra měla podobné rysy a zachránil jsem si život jen proto, že byla jedinou neustálou řadou ústupů: MHD v roce 1972 (když jsem opustil Institut pro mechaniku tekutin v Marseille, kde jsem v roce 1967 přivedl laboratoř na vrchol mezinárodního výzkumu), informatika v roce 1983 (byl jsem podříditelem informačního oddělení Univerzity v Provence), výuka na fakultě humanitních a matematických věd (obrácení koule, Pour la Science 1979), návrat do MHD (1975–1986), opuštění vydavatelské činnosti komiksu v roce 1990, rychlé opuštění v letech 2000 v egyptologii. V současnosti téměř úplné opuštění nebo vážná přestávka ve fyzice hvězd, kosmologii a matematické fyzice kvůli nedostatku pozitivních reakcí (1985–2008).
V současnosti návrat s Savoir sans Frontières a znovuvydání knih a komiksů. Aktivity na okraji opuštění v MHD a téma OVNIs. Níže fotografie MHD stolu ve stavbě v Rochefortu (stav květen 2010):
Je to styl Algeco Jacques, ve dvorku INSERM, s tím rozdílem, že se o to nezabývám já, ale statečný technik ve věku 40 let. Na rozdíl od Bernarda Palissy nezahoruji své nábytek.
Francouzská špičková MHD, MHD „mimo rovnováhu“, ta „dvouteplotní plazma“, která nám umožňuje být na prvním místě na mezinárodních konferencích (Vilnius 2008, Bremen 2009), tady je!
Bylo by komické, kdyby to nebylo naprosto smutné
K příležitosti roku fyziky vydala revue Courrier du CNRS brožuru s deseti nerozhodnutými problémy ve vědě. Jedna z těchto otázek se týká struktury vody ve všech jejích stavech. Níže reprodukce tohoto materiálu.

 | Zatím fyzici úspěšně pozorovali, že se vytvářejí a zánikají bez přestání – každá žije průměrně jednu miliardtinu miliardiny sekundy, velké množství se tvoří a je třeba, aby byly tři atomy dokonale zarovnány, aby vznikla vazba. Z každého kapalného látky je voda jediná, která splňuje tyto tři charakteristiky. A právě to vysvětluje část známých anomálií popsaných výzkumníky: na jedné straně voda není plyn při pokojové teplotě, protože vodíkové vazby jsou dostatečně silné. Voda tedy má velkou kohezi. Výsledek: je třeba dodat mnoho energie, aby se tyto vazby přerušily, což vysvětluje, proč vaří až při 100 °C. Na druhé straně to ale není ani pevná látka při pokojové teplotě, protože vazby jsou stále křehké. |
| Zatím fyzici úspěšně pozorovali, že se vytvářejí a zánikají bez přestání – každá žije průměrně jednu miliardtinu miliardiny sekundy, velké množství se tvoří a je třeba, aby byly tři atomy dokonale zarovnány, aby vznikla vazba. Z každého kapalného látky je voda jediná, která splňuje tyto tři charakteristiky. A právě to vysvětluje část známých anomálií popsaných výzkumníky: na jedné straně voda není plyn při pokojové teplotě, protože vodíkové vazby jsou dostatečně silné. Voda tedy má velkou kohezi. Výsledek: je třeba dodat mnoho energie, aby se tyto vazby přerušily, což vysvětluje, proč vaří až při 100 °C. Na druhé straně to ale není ani pevná látka při pokojové teplotě, protože vazby jsou stále křehké. |
|---|
** | P | ro
| P | ro
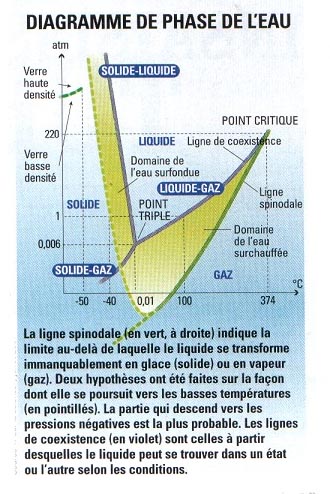
José Teixeira je hlubší poznání dynamiky vodíkové vazby nezbytné, pokud chceme někdy skutečně pochopit vodu. Bernard Cabane jde stejným směrem: „Stále nám chybí mnoho informací o vodě, abychom měli realistický a předpovídající model jejího chování. I když známe povahu vazeb mezi molekulami, dokud nebudeme vědět, jak se izolovaná molekula interaguje nejen s prvními sousedy, ale i s ostatními, model nebude dobrý.“ A současné počítačové simulace mu dávají pravdu. Ve skutečnosti pokud se pokusíme vysvětlit tři hlavní zvláštní anomálie vody, modely reprodukují jen jednu nebo dvě. Nikdy všechny tři najednou. Vodíková vazba: vzniká mezi dvěma stejnými nebo různými molekulami. Deficit náboje na atomu vodíku umožňuje vznik vazby. Ale fyzici nemají nedostatek nápadů, aby záhadu odhalili. Proto studují její strukturu při nízkých teplotách. „Vodíkové vazby jsou stabilnější pod 0 °C“, vysvětluje José Teixeira. Můžeme tedy pokusit se lépe pochopit kapalinu, pokud sledujeme její vývoj až do -40 °C.“ Kapalná až do -40 °C? Ano, pokud je zbavena všech nečistot, jinak okamžitě krystalizuje. Vědci to nazývají
přehřátí
| (podívejte se na fázový diagram), což existuje i u jiných kapalin, jako je toluen, gallium nebo roztavená křemík. „Zatím rekord pro vodu je -42 °C – o trochu lépe než pro přehřátou vodu v některých atmosférických mracích“, upřesňuje Frédéric Caupin, výzkumník na Laboratoři statistické fyziky ENS. Pod -40 °C je už jen tepelná agitace molekul vody dostačující k tomu, aby kapalina přešla v led. Po překročení této teplotní bariéry má kapalná voda extrémně krátkou životnost. Fyzici pak nemají možnost ji pozorovat. |
|---|
Přibližně kolem -130 °C se objevuje další zajímavý jev: pokud je voda dostatečně rychle ochlazena až do této teploty, převede se na amorfní led, tedy má strukturu skla (viz str. 16). Zjevně se ukazuje: „O struktuře vody mezi -40 °C a -130 °C nic nevíme“, přiznává José Teixeira. S troškou humoru výzkumníci tuto oblast nazývají „nevyhnutelné území“. Překvapení v roce 1984: fyzici Mishima, Calvert a Whalley objevili druhý druh amorfního ledu, hustší než první, stlačením běžného ledu při velmi nízké teplotě. Výsledek znovu probudil starší myšlenky. Už v roce 1892 navrhoval Röntgen, že voda je směs kapaliny a ledu. Dnes někteří vidí v objevu dvou druhů amorfního ledu slibnou cestu: voda by mohla být alespoň při nízkých teplotách směsí dvou kapalin, jedné s nízkou hustotou a druhé s vysokou hustotou. Tato myšlenka trochu zpochybňuje José Teixeira. A navrhuje, že viníkem je stále a znovu vodíková vazba. Ale jak rozhodnout, když „nevyhnutelné území“ zůstává nedostupné pro měření? Řešení: vylepšit experimenty tzv. kavitace, které probíhají při pokojové teplotě a při „záporných“ tlacích.
Pro José Teixeira je hlubší poznání dynamiky vodíkové vazby nezbytné, pokud chceme někdy skutečně pochopit vodu. Bernard Cabane jde stejným směrem: „Stále nám chybí mnoho informací o vodě, abychom měli realistický a předpovídající model jejího chování. I když známe povahu vazeb mezi molekulami, dokud nebudeme vědět, jak se izolovaná molekula interaguje nejen s prvními sousedy, ale i s ostatními, model nebude dobrý.“ A současné počítačové simulace mu dávají pravdu. Ve skutečnosti pokud se pokusíme vysvětlit tři hlavní zvláštní anomálie vody, modely reprodukují jen jednu nebo dvě. Nikdy všechny tři najednou. Vodíková vazba: vzniká mezi dvěma stejnými nebo různými molekulami. Deficit náboje na atomu vodíku umožňuje vznik vazby. Ale fyzici nemají nedostatek nápadů, aby záhadu odhalili. Proto studují její strukturu při nízkých teplotách. „Vodíkové vazby jsou stabilnější pod 0 °C“, vysvětluje José Teixeira. Můžeme tedy pokusit se lépe pochopit kapalinu, pokud sledujeme její vývoj až do -40 °C.“ Kapalná až do -40 °C? Ano, pokud je zbavena všech nečistot, jinak okamžitě krystalizuje. Vědci to nazývají
přehřátí
(podívejte se na fázový diagram), což existuje i u jiných kapalin, jako je toluen, gallium nebo roztavená křemík. „Zatím rekord pro vodu je -42 °C – o trochu lépe než pro přehřátou vodu v některých atmosférických mracích“, upřesňuje Frédéric Caupin, výzkumník na Laboratoři statistické fyziky ENS. Pod -40 °C je už jen tepelná agitace molekul vody dostačující k tomu, aby kapalina přešla v led. Po překročení této teplotní bariéry má kapalná voda extrémně krátkou životnost. Fyzici pak nemají možnost ji pozorovat.
Pro José Teixeira je hlubší poznání dynamiky vodíkové vazby nezbytné, pokud chceme někdy skutečně pochopit vodu. Bernard Cabane jde stejným směrem: „Stále nám chybí mnoho informací o vodě, abychom měli realistický a předpovídající model jejího chování. I když známe povahu vazeb mezi molekulami, dokud nebudeme vědět, jak se izolovaná molekula interaguje nejen s prvními sousedy, ale i s ostatními, model nebude dobrý.“ A současné počítačové simulace mu dávají pravdu. Ve skutečnosti pokud se pokusíme vysvětlit tři hlavní zvláštní anomálie vody, modely reprodukují jen jednu nebo dvě. Nikdy všechny tři najednou. Vodíková vazba: vzniká mezi dvěma stejnými nebo různými molekulami. Deficit náboje na atomu vodíku umožňuje vznik vazby. Ale fyzici nemají nedostatek nápadů, aby záhadu odhalili. Proto studují její strukturu při nízkých teplotách. „Vodíkové vazby jsou stabilnější pod 0 °C“, vysvětluje José Teixeira. Můžeme tedy pokusit se lépe pochopit kapalinu, pokud sledujeme její vývoj až do -40 °C.“ Kapalná až do -40 °C? Ano, pokud je zbavena všech nečistot, jinak okamžitě krystalizuje. Vědci to nazývají
přehřátí
(podívejte se na fázový diagram), což existuje i u jiných kapalin, jako je toluen, gallium nebo roztavená křemík. „Zatím rekord pro vodu je -42 °C – o trochu lépe než pro přehřátou vodu v některých atmosférických mracích“, upřesňuje Frédéric Caupin, výzkumník na Laboratoři statistické fyziky ENS. Pod -40 °C je už jen tepelná agitace molekul vody dostačující k tomu, aby kapalina přešla v led. Po překročení této teplotní bariéry má kapalná voda extrémně krátkou životnost. Fyzici pak nemají možnost ji pozorovat.

| Z | koušejí
| kohézi vody, hledají maximální tah, který lze aplikovat na kapalinu pomocí ultrazvuku před vznikem první bubliny páry. „Naděje je dosáhnout tlaku -1400 barů“, komentuje Frédéric Caupin. Pak bychom měli nové údaje, které by umožnily vyloučit určité hypotézy o struktuře vody.“ Bohužel jsou tyto experimenty dnes velmi obtížné provést. Ještě je třeba dosáhnout pokroku ve čištění vody. Takže trpělivost. Záhadu vody budou výzkumníci řešit ještě mnoho let, říká Julien Bourdet. K odhalení záhad vody fyzici spoléhají na experimenty kavitace (zde provedené v hydraulickém tunelu), kdy se objevují bubliny páry. |
|---|
Mezi anomáliemi vody jsou tři hlavní:
-
velmi silná koheze, což se projevuje vysokými teplotami tání a varu;
-
vysoká dielektrická konstanta, která jí umožňuje rozpouštět všechny soli.
K odhalení záhad vody fyzici spoléhají na experimenty kavitace (zde provedené v hydraulickém tunelu), kdy se objevují bubliny páry
- velká expanze při nízkých teplotách (pod 4 °C) a také při krystalizaci.
Stejně jako lze najít přehřátou vodu, lze najít i přehřátou vodu, tedy kapalinu nad 100 °C. Vznik explozivní bubliny se nazývá kavitace. Snížení tlaku je ekvivalentem ohřátí vody. Výzkumníci vytahují vodu (mluví o záporném tlaku), dokud neobjeví první bublinu páry.
Julien Bourdet
KONTAKTY
Bernard Cabane: bcabane @ pmmh.espci.fr Frédéric Caupin: caupin @ lps.ens.fr José Teixeira: teix@ Ilb.saclay.ceafr

Mezi anomáliemi vody jsou tři hlavní:
-
velmi silná koheze, což se projevuje vysokými teplotami tání a varu;
-
vysoká dielektrická konstanta, která jí umožňuje rozpouštět všechny soli.
K odhalení záhad vody fyzici spoléhají na experimenty kavitace (zde provedené v hydraulickém tunelu), kdy se objevují bubliny páry
Mezi anomáliemi vody jsou tři hlavní:
-
velmi silná koheze, což se projevuje vysokými teplotami tání a varu;
-
vysoká dielektrická konstanta, která jí umožňuje rozpouštět všechny soli.
K odhalení záhad vody fyzici spoléhají na experimenty kavitace (zde provedené v hydraulickém tunelu), kdy se objevují bubliny páry
Více o názoru CNRS na práce Jean-Pierre Petit
Zpět k přehledu Zpět na úvodní stránku
Počet návštěv této stránky od 8. března 2005: