Η άποψη του CNRS για τις εργασίες του Τζακ Μπενβενίστε
Έξι μήνες μετά το θάνατό του, η άποψη του CNRS για τις εργασίες του Τζακ Μπενβενίστε
8 Μαρτίου 2005
Σε πρόλογο:



**
[Το ηχητικό αρχείο της συνέντευξης του Μοντανιέρ, Μάιος 2010](../../AUDIOS/LE SEPT NEUF DU DIMANCHE 02.05.2010_benveniste.mp3)
10 Μαΐου 2010.
Ένας αναγνώστης μου έστειλε ένα τμήμα μιας εκπομπής όπου ακούγεται ο Λουκ Μοντανιέρ, ο Νομπελίστας της Ιατρικής, να επαινεί τον εκτελεσμένο φίλο μου Τζακ Μπενβενίστε.
Ο καθηγητής Λουκ Μοντανιέρ, Νομπελίστας της Ιατρικής, το 2007, στο Λουγκάνο, αυτός δεν προχωρεί με το πίσω μέρος της κουτάλας και δεν διστάζει να δηλώσει ότι ο Τζακ ήταν ένας εξαιρετικός πρωτοπόρος, προηγμένος για την εποχή του, και η πεποίθησή του ότι θα αναγνωριστεί η ορθότητα των απόψεών του κάποια μέρα.
Μνήμης θυμάμαι την εποχή που ο γενικός διευθυντής του ΙΝΣΕΡΜ, Λαζάρε, έβγαλε από τον Τζακ τα 200 τετραγωνικά μέτρα των χώρων του ΙΝΣΕΡΜ 200 στο Κλαμαρτ, πράγμα που τον οδήγησε να μεταφορτωθεί στα κατασκευαστικά φορτηγά στην αυλή! Μια απόλυτη αισχύνη.
Πολλές φορές είχα πει στον Τζακ "παρατήρησε, θα χάσεις τη ζωή σου!" Αλλά προσπάθησε, προσπάθησε, μέχρι την τελευταία του ανάσα, μέχρι να χάσει τη ζωή του, με την καρδιά στα θραύσματα.
Η καριέρα μου έχει παρουσιάσει παρόμοια στοιχεία και τη ζωή μου τη χάρησα μόνο γιατί ήταν μια συνεχόμενη αλυσίδα αποχωρήσεων: ΜΗΔ το 1972 (αφήνοντας το εργαστήριο που είχα φέρει το 1967 στο Μαρσέιλλε στο επίπεδο της διεθνούς επιστήμης), Πληροφορική το 1983 (ήμουν αντιδιευθυντής του τμήματος πληροφορικής του πανεπιστημίου της Προβηγκίας), διδασκαλία στο πανεπιστήμιο των Ανθρωπιστικών Επιστημών, μαθηματικά (αναστροφή της σφαίρας, Pour la Science 1979), ένα επαναπροσανατολισμός στο ΜΗΔ (1975-1986), απόρριψη της έκδοσης κόμικς από έναν εκδότη το 1990, γρήγορη απόρριψη στις χιλιάδες των ετών, στην αρχαιολογία. Τώρα, σχεδόν απόρριψη, ή σοβαρή αναστολή στην αστροφυσική, την κοσμολογία και τη μαθηματική φυσική, λόγω αρνητικών αντιδράσεων (1985-2008).
Τώρα, ένας αναπόδειξη με το Σαβουάρ Σαν Φροντιέρς και την επανέκδοση βιβλίων και κόμικς. Απορριπτικές δραστηριότητες στο ΜΗΔ και το θέμα των ΟΒΝΙ. Παρακάτω η φωτογραφία του χώρου ΜΗΔ σε εγκατάσταση στο Ροσέφορτ (κατάσταση τον Μάιο 2010) :
Αυτό είναι στο στυλ των Αλγεκό του Τζακ, στην αυλή του ΙΝΣΕΡΜ, με τη διαφορά ότι δεν το αναλαμβάνω εγώ, αλλά ένας θρασύς τεχνικός 40 ετών. Αντίθετα με τον Μπερνάρ Παλίσι, δεν θα καίω τα καθήσια μου.
Η προοδευτική ΜΗΔ της Γαλλίας, η ΜΗΔ "εκτός ισορροπίας", αυτή των "διπλών θερμοκρασιών πλασμάτων", που μας επιτρέπει να βρεθούμε στην κορυφή σε διεθνή συνέδρια (Vilnius 2008, Bremen 2009), αυτή είναι!
Θα ήταν χαριτωμένο αν δεν ήταν τόσο θλιβερό
Στο πλαίσιο της Ετήσιας Φυσικής, το περιοδικό Το Κορρεσποντ του CNRS δημοσίευσε ένα φυλλάδιο που παρουσιάζει δέκα προβλήματα που δεν έχουν λυθεί στην επιστήμη. Ένα από αυτά τα θέματα αφορά τη δομή του νερού, σε όλες τις μορφές του. Παρακάτω η αναπαραγωγή αυτού του φακέλου.

 | Μέχρι στιγμής, οι φυσικοί έχουν καταφέρει να παρατηρήσουν ότι δημιουργούνται και καταστρέφονται συνεχώς - κάθε μία ζει στο μέσο όρο ένα χιλιοστό του δισεκατομμυριοστού του δευτερολέπτου, ότι πολλές από αυτές δημιουργούνται και ότι χρειάζεται να είναι τα τρία άτομα που συμμετέχουν τέλεια στη σειρά για να εμφανιστεί μια σύνδεση. Ωστόσο, από όλα τα υγρά, το νερό είναι το μόνο που συνδυάζει αυτές τις τρεις ιδιότητες. Και αυτό είναι πιθανόν το πρόσθετο που εξηγεί κατά μεγάλο βαθμό τις φημισμένες ανωμαλίες που περιγράφουν οι ερευνητές: από τη μια πλευρά, το νερό δεν είναι αέριο σε θερμοκρασία περιβάλλοντος, γιατί οι δεσμοί υδρογόνου είναι αρκετά ισχυροί. Το νερό είναι, επομένως, διαθέσιμο με μεγάλη δύναμη συνοχής. Αποτέλεσμα: χρειάζεται πολύ ενέργεια για να διαλυθούν αυτοί οι δεσμοί, που εξηγεί ότι βράζει μόνο στους 100 °C. Από την άλλη πλευρά, δεν είναι ούτε στερεό σε θερμοκρασία περιβάλλοντος, γιατί οι δεσμοί είναι όμως ακόμη ευαίσθητοι. |
| Μέχρι στιγμής, οι φυσικοί έχουν καταφέρει να παρατηρήσουν ότι δημιουργούνται και καταστρέφονται συνεχώς - κάθε μία ζει στο μέσο όρο ένα χιλιοστό του δισεκατομμυριοστού του δευτερολέπτου, ότι πολλές από αυτές δημιουργούνται και ότι χρειάζεται να είναι τα τρία άτομα που συμμετέχουν τέλεια στη σειρά για να εμφανιστεί μια σύνδεση. Ωστόσο, από όλα τα υγρά, το νερό είναι το μόνο που συνδυάζει αυτές τις τρεις ιδιότητες. Και αυτό είναι πιθανόν το πρόσθετο που εξηγεί κατά μεγάλο βαθμό τις φημισμένες ανωμαλίες που περιγράφουν οι ερευνητές: από τη μια πλευρά, το νερό δεν είναι αέριο σε θερμοκρασία περιβάλλοντος, γιατί οι δεσμοί υδρογόνου είναι αρκετά ισχυροί. Το νερό είναι, επομένως, διαθέσιμο με μεγάλη δύναμη συνοχής. Αποτέλεσμα: χρειάζεται πολύ ενέργεια για να διαλυθούν αυτοί οι δεσμοί, που εξηγεί ότι βράζει μόνο στους 100 °C. Από την άλλη πλευρά, δεν είναι ούτε στερεό σε θερμοκρασία περιβάλλοντος, γιατί οι δεσμοί είναι όμως ακόμη ευαίσθητοι. |
|---|
** | Π | ουρ
| Π | ουρ
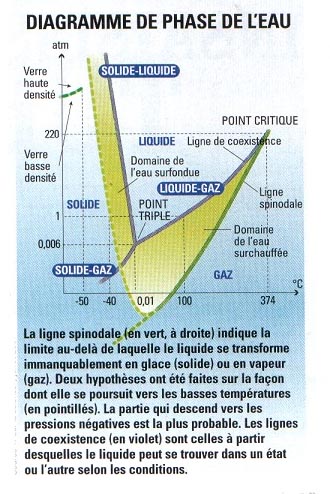
| για τον Ζοζέ Τειξειρά, μια πιο βαθιά γνώση της δυναμικής του δεσμού υδρογόνου είναι απαραίτητη αν θέλουμε πραγματικά να κατανοήσουμε το νερό κάποια στιγμή. Ο Μπερνάρ Καμπάνε πάει επίσης σε αυτή την κατεύθυνση: « Ακόμα χρειαζόμαστε πολλές πληροφορίες για το νερό για να έχουμε ένα πραγματικό και προβλέψιμο μοντέλο για τη συμπεριφορά του. Ακόμα κι αν γνωρίζουμε τη φύση των δεσμών μεταξύ των μορίων, μέχρι να μάθουμε πώς ένα μόριο μόνο αλληλεπιδρά όχι μόνο με τους πρώτους γείτονές του αλλά και με τα άλλα, τότε το μοντέλο δεν θα είναι καλό. . Και οι τρέχουσες υπολογιστικές προσομοιώσεις τους δίνουν δίκιο. Πράγματι, αν προσπαθήσουμε να εξηγήσουμε τις τρεις κύριες ιδιαίτερες ανωμαλίες του νερού, τα μοντέλα αναπαράγουν μόνο μία ή δύο. Ποτέ τρεις ταυτόχρονα. Δεσμός υδρογόνου: αυτός προκύπτει μεταξύ δύο μορίων, ταυτόσημων ή όχι. Είναι το έλλειμμα φορτίου που φέρει το άτομο του υδρογόνου που επιτρέπει την εμφάνιση του δεσμού. Αλλά οι φυσικοί δεν έχουν έλλειψη ιδεών για να αποκαλύψουν το μυστικό. Για να το κάνουν αυτό, μελετούν τη δομή του σε χαμηλές θερμοκρασίες. « Οι δεσμοί υδρογόνου είναι πιο σταθεροί κάτω από τους 0 °C, δηλώνει ο Ζοζέ Τειξειρά. Μπορούμε τότε να προσπαθήσουμε να κατανοήσουμε καλύτερα το υγρό νερό αν ακολουθήσουμε την εξέλιξή του μέχρι τους - 40 °C. » Υγρό μέχρι -40 °C; Ναι, αν είναι απαλλαγμένο από όλες τις ακαθαρσίες, διαφορετικά κρυσταλλώνει αμέσως. Οι επιστήμονες το ονομάζουν υπερψύξη (βλ. διάγραμμα φάσης), το οποίο υπάρχει επίσης για άλλα υγρά, όπως το τολουόλιο, το γαλλιούχο ή το ζεστό πυρίτιο. « Μέχρι στιγμής, το ρεκόρ για το νερό είναι στους - 42 °C - ελάχιστα καλύτερα από το υπερψυγμένο νερό που υπάρχει σε ορισμένα ατμοσφαιρικά σύννεφα, δηλώνει ο Φρεντερίκ Καουπίν, ερευνητής στο Εργαστήριο Στατιστικής Φυσικής της ΕΝΣ. Κάτω από τους - 40 °C, αρκεί η θερμική διαταραχή των μορίων του νερού για να μετατραπεί το υγρό σε πάγο. Μετά την πάροδο αυτής της θερμοκρασιακής φράγματος, η διάρκεια ζωής του υγρού νερού γίνεται εξαιρετικά σύντομη. Οι φυσικοί δεν έχουν τώρα τη δυνατότητα να το παρατηρήσουν. |
|---|
Περίπου στους -130 °C εμφανίζεται ένα άλλο ενδιαφέρον φαινόμενο: αν το νερό ψυχρανθεί αρκετά γρήγορα μέχρι αυτή τη θερμοκρασία, μετατρέπεται σε αμορφούς πάγο, δηλαδή έχει τη δομή του γυαλιού (βλ. σελ. 16). Μια παρατήρηση που επιβεβαιώνει « Δεν ξέρουμε τίποτα για τη δομή του νερού μεταξύ - 40 °C και -130 °C », αναγνωρίζει ο Ζοζέ Τειξειρά. Χωρίς να το παρακολουθεί χωρίς χιλιάδες, οι ερευνητές το ονομάζουν το « μη έδαφος ». Ανατροπή το 1984: οι φυσικοί Μισίμα, Καλβέρτ και Χάλι έβρισκαν μια δεύτερη μορφή πάγου, αμορφωτική, πιο πυκνή από την πρώτη, πιέζοντας τον συνηθισμένο πάγο σε πολύ χαμηλή θερμοκρασία. Ένα αποτέλεσμα που επανέφερε παλιές ιδέες. Πράγματι, το 1892, Ρόντεν έθεσε την υπόθεση ότι το νερό ήταν ένα μίγμα υγρού και πάγου. Σήμερα, ορισμένοι βλέπουν στην ανακάλυψη των δύο μορφών αμορφωτικού πάγου μια υποσχετική πορεία: το νερό θα ήταν, τουλάχιστον σε χαμηλές θερμοκρασίες, ένα μίγμα δύο υγρών, του ενός με χαμηλή πυκνότητα και του άλλου με υψηλή πυκνότητα. Μια ιδέα που αφήνει λίγο αμφισβητήσιμο τον Ζοζέ Τειξειρά. Και προτείνει ότι ο υπεύθυνος είναι πάλι και πάλι ο δεσμός υδρογόνου. Αλλά πώς να το αποφασίσουμε, όταν το μη έδαφος παραμένει απροσπέλαστο για τις μετρήσεις; Μια λύση: βελτιώνοντας τις πειραματικές εργασίες που ονομάζονται καβιτάτιο, που διεξάγονται σε θερμοκρασία περιβάλλοντος και σε πιέσεις που χαρακτηρίζονται ως « αρνητικές » .
για τον Ζοζέ Τειξειρά, μια πιο βαθιά γνώση της δυναμικής του δεσμού υδρογόνου είναι απαραίτητη αν θέλουμε πραγματικά να κατανοήσουμε το νερό κάποια στιγμή. Ο Μπερνάρ Καμπάνε πάει επίσης σε αυτή την κατεύθυνση: « Ακόμα χρειαζόμαστε πολλές πληροφορίες για το νερό για να έχουμε ένα πραγματικό και προβλέψιμο μοντέλο για τη συμπεριφορά του. Ακόμα κι αν γνωρίζουμε τη φύση των δεσμών μεταξύ των μορίων, μέχρι να μάθουμε πώς ένα μόριο μόνο αλληλεπιδρά όχι μόνο με τους πρώτους γείτονές του αλλά και με τα άλλα, τότε το μοντέλο δεν θα είναι καλό. . Και οι τρέχουσες υπολογιστικές προσομοιώσεις τους δίνουν δίκιο. Πράγματι, αν προσπαθήσουμε να εξηγήσουμε τις τρεις κύριες ιδιαίτερες ανωμαλίες του νερού, τα μοντέλα αναπαράγουν μόνο μία ή δύο. Ποτέ τρεις ταυτόχρονα. Δεσμός υδρογόνου: αυτός προκύπτει μεταξύ δύο μορίων, ταυτόσημων ή όχι. Είναι το έλλειμμα φορτίου που φέρει το άτομο του υδρογόνου που επιτρέπει την εμφάνιση του δεσμού. Αλλά οι φυσικοί δεν έχουν έλλειψη ιδεών για να αποκαλύψουν το μυστικό. Για να το κάνουν αυτό, μελετούν τη δομή του σε χαμηλές θερμοκρασίες. « Οι δεσμοί υδρογόνου είναι πιο σταθεροί κάτω από τους 0 °C, δηλώνει ο Ζοζέ Τειξειρά. Μπορούμε τότε να προσπαθήσουμε να κατανοήσουμε καλύτερα το υγρό νερό αν ακολουθήσουμε την εξέλιξή του μέχρι τους - 40 °C. » Υγρό μέχρι -40 °C; Ναι, αν είναι απαλλαγμένο από όλες τις ακαθαρσίες, διαφορετικά κρυσταλλώνει αμέσως. Οι επιστήμονες το ονομάζουν υπερψύξη (βλ. διάγραμμα φάσης), το οποίο υπάρχει επίσης για άλλα υγρά, όπως το τολουόλιο, το γαλλιούχο ή το ζεστό πυρίτιο. « Μέχρι στιγμής, το ρεκόρ για το νερό είναι στους - 42 °C - ελάχιστα καλύτερα από το υπερψυγμένο νερό που υπάρχει σε ορισμένα ατμοσφαιρικά σύννεφα, δηλώνει ο Φρεντερίκ Καουπίν, ερευνητής στο Εργαστήριο Στατιστικής Φυσικής της ΕΝΣ. Κάτω από τους - 40 °C, αρκεί η θερμική διαταραχή των μορίων του νερού για να μετατραπεί το υγρό σε πάγο. Μετά την πάροδο αυτής της θερμοκρασιακής φράγματος, η διάρκεια ζωής του υγρού νερού γίνεται εξαιρετικά σύντομη. Οι φυσικοί δεν έχουν τώρα τη δυνατότητα να το παρατηρήσουν.
για τον Ζοζέ Τειξειρά, μια πιο βαθιά γνώση της δυναμικής του δεσμού υδρογόνου είναι απαραίτητη αν θέλουμε πραγματικά να κατανοήσουμε το νερό κάποια στιγμή. Ο Μπερνάρ Καμπάνε πάει επίσης σε αυτή την κατεύθυνση: « Ακόμα χρειαζόμαστε πολλές πληροφορίες για το νερό για να έχουμε ένα πραγματικό και προβλέψιμο μοντέλο για τη συμπεριφορά του. Ακόμα κι αν γνωρίζουμε τη φύση των δεσμών μεταξύ των μορίων, μέχρι να μάθουμε πώς ένα μόριο μόνο αλληλεπιδρά όχι μόνο με τους πρώτους γείτονές του αλλά και με τα άλλα, τότε το μοντέλο δεν θα είναι καλό. . Και οι τρέχουσες υπολογιστικές προσομοιώσεις τους δίνουν δίκιο. Πράγματι, αν προσπαθήσουμε να εξηγήσουμε τις τρεις κύριες ιδιαίτερες ανωμαλίες του νερού, τα μοντέλα αναπαράγουν μόνο μία ή δύο. Ποτέ τρεις ταυτόχρονα. Δεσμός υδρογόνου: αυτός προκύπτει μεταξύ δύο μορίων, ταυτόσημων ή όχι. Είναι το έλλειμμα φορτίου που φέρει το άτομο του υδρογόνου που επιτρέπει την εμφάνιση του δεσμού. Αλλά οι φυσικοί δεν έχουν έλλ