opinione del CNRS sui lavori di Jacques Benveniste
Sei mesi dopo la sua morte, l'opinione del CNRS sui lavori di J. Benveniste
8 marzo 2005
In prefazione:



**
[Il file audio dell'intervista a Montagnier, maggio 2010](../../AUDIOS/LE SEPT NEUF DU DIMANCHE 02.05.2010_benveniste.mp3)
10 maggio 2010.
Un lettore mi ha inviato un estratto di un programma radiofonico in cui si sente il premio Nobel Luc Montagnier lodare il mio sfortunato amico Jacques Benveniste.
Il professor Luc Montagnier, premio Nobel per la medicina nel 2007 a Lugano, non si tira indietro e dichiara senza mezzi termini che Jacques fu un geniale precursore, in anticipo sui tempi, e che è convinto che un giorno si riconoscerà la correttezza delle sue idee.
Ricordo l'epoca in cui il direttore generale dell'INSERM, Lazare, aveva tolto a Jacques i suoi 200 metri quadrati di spazio all'INSERM 200 di Clamart, costringendolo a trasferirsi nei baracconi Algeco nel cortile! Una vera vergogna.
Molte volte ho detto a Jacques: "abbandona, rischierai di morire per questo!" Ma lui si è aggrappato, si è aggrappato fino all'ultimo respiro, fino a lasciarci la vita, il cuore spezzato.
La mia carriera ha presentato aspetti simili e sono dovuto uscirne vivo solo perché è stata una serie ininterrotta di abbandoni: MHD nel 1972 (abbandonando all'Istituto di Meccanica dei Fluidi di Marsiglia l'installazione con cui avevo portato nel 1967 il laboratorio al vertice a livello internazionale), Informatica nel 1983 (ero sottodirettore del servizio informatico dell'Università di Provenza), insegnamento in facoltà di lettere e matematica (inversione della sfera, Pour la Science 1979), un ritorno in MHD (1975-1986), abbandono della pubblicazione di fumetti da parte di un editore nel 1990, abbandono rapido negli anni duemila in egittologia. Al momento, quasi abbandono o seria sospensione in astrofisica, cosmologia e fisica matematica, a causa della mancanza di riscontri positivi (1985-2008).
Attualmente, un nuovo slancio con Savoir sans Frontières e riedizione di libri e fumetti. Attività al limite dell'abbandono in MHD e argomento OVNIs. Di seguito la foto del banco MHD in fase di montaggio a Rochefort (stato a maggio 2010):
È nello stile degli Algeco di Jacques, nel cortile dell'INSERM, con la differenza che non sono io a occuparmene, ma un coraggioso tecnico di 40 anni. A differenza di Bernard Palissy, non brucerò i miei mobili.
La MHD francese di punta, la MHD "fuori equilibrio", quella dei "plasmi bitemperatura", che ci permette di figurare al primo posto in convegni internazionali (Vilnius 2008, Brema 2009), eccola qui!
Sarebbe comico se non fosse una tristezza assoluta.
In occasione dell'Anno della Fisica, la rivista Le Courrier du CNRS ha pubblicato un opuscolo presentando dieci problemi irrisolti nella scienza. Una di queste domande riguarda la struttura dell'acqua in tutti i suoi stati. Di seguito la riproduzione di questo dossier.

 | Per il momento, i fisici sono riusciti a osservare che si creano e si distruggono continuamente – ognuna vive in media un millesimo di miliardesimo di secondo, che un gran numero di esse si forma e che è necessario che i tre atomi coinvolti siano perfettamente allineati affinché si stabilisca un legame. Ora, tra tutti i liquidi, l'acqua è l'unico a possedere queste tre caratteristiche. Ed è probabilmente questo che spiega in parte le famose anomalie descritte dai ricercatori: da una parte, l'acqua non è un gas a temperatura ambiente, perché i legami idrogeno sono abbastanza forti. L'acqua quindi possiede una grande coesione. Risultato: è necessario apportare molta energia per rompere questi legami, il che spiega perché bolle solo a 100 °C. Dall'altra parte, non è neanche un solido a temperatura ambiente, perché i legami sono comunque fragili. |
| Per il momento, i fisici sono riusciti a osservare che si creano e si distruggono continuamente – ognuna vive in media un millesimo di miliardesimo di secondo, che un gran numero di esse si forma e che è necessario che i tre atomi coinvolti siano perfettamente allineati affinché si stabilisca un legame. Ora, tra tutti i liquidi, l'acqua è l'unico a possedere queste tre caratteristiche. Ed è probabilmente questo che spiega in parte le famose anomalie descritte dai ricercatori: da una parte, l'acqua non è un gas a temperatura ambiente, perché i legami idrogeno sono abbastanza forti. L'acqua quindi possiede una grande coesione. Risultato: è necessario apportare molta energia per rompere questi legami, il che spiega perché bolle solo a 100 °C. Dall'altra parte, non è neanche un solido a temperatura ambiente, perché i legami sono comunque fragili. |
|---|
** | P | er
| P | er
José Teixeira, una conoscenza più approfondita della dinamica del legame idrogeno è indispensabile se si vuole davvero capire un giorno l'acqua. Bernard Cabane va anch'egli in questa direzione: « Ci mancano ancora molte informazioni sull'acqua per avere un modello realistico e predittivo del suo comportamento. Anche se conosciamo la natura dei legami tra molecole, finché non sapremo come una molecola isolata interagisce non solo con le prime vicine ma anche con le altre, il modello non sarà buono.» E le attuali simulazioni numeriche gli danno ragione. Infatti, se si cerca di spiegare le tre principali anomalie particolari dell'acqua, i modelli ne riproducono solo una o due. Mai tutte e tre contemporaneamente. Legame idrogeno: si stabilisce tra due molecole uguali o diverse. È il difetto di carica portato dall'atomo di idrogeno che permette l'apparizione del legame. Ma i fisici non mancano di idee per tentare di sciogliere il mistero. Per questo studiano la sua struttura a freddo. « I legami idrogeno sono più stabili al di sotto dei 0 °C», spiega José Teixeira. Si può quindi cercare di capire meglio l'acqua liquida seguendone l'evoluzione fino a -40 °C. Liquida fino a -40 °C? Sì, se è privata di tutte le impurità, altrimenti si cristallizza immediatamente. I ricercatori chiamano questo fenomeno la
superficie
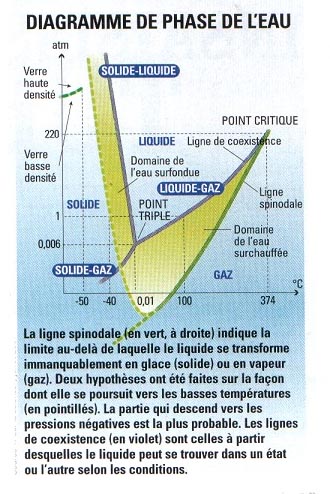
| (vedi diagramma di fase), che esiste anche per altri liquidi, come il toluene, il gallio o il silicio fuso. « Al momento, il record per l'acqua è a -42 °C – appena meglio dell'acqua surriscaldata presente in alcuni nuvole atmosferiche», precisa Frédéric Caupin, ricercatore al Laboratorio di Fisica Statistica dell'ENS. Al di sotto dei -40 °C, basta l'agitazione termica delle molecole d'acqua perché il liquido si trasformi in ghiaccio. Superata questa barriera di temperatura, la durata di vita dell'acqua liquida diventa estremamente breve. I fisici non hanno più modo di osservarla. |
|---|
È intorno ai -130 °C che si verifica un altro fenomeno interessante: se l'acqua viene raffreddata abbastanza velocemente fino a questa temperatura, si trasforma in ghiaccio amorfo, cioè ha la struttura del vetro (vedi p. 16). Una constatazione si impone: « Non sappiamo nulla sulla struttura dell'acqua tra i -40 °C e i -130 °C», ammette José Teixeira. Senza troppo umorismo, i ricercatori chiamano questa zona il « terra di nessuno ». Svolta nel 1984: i fisici Mishima, Calvert e Whalley scoprono una seconda forma di ghiaccio amorfo, più densa della prima, comprimendo il ghiaccio ordinario a temperature molto basse. Un risultato che ha fatto rinascere vecchie ipotesi. Infatti, nel 1892, Röntgen aveva avanzato l'ipotesi che l'acqua fosse un miscuglio di liquido e ghiaccio. Oggi alcuni vedono nella scoperta delle due forme di ghiaccio amorfo una pista promettente: l'acqua sarebbe, almeno a basse temperature, un miscuglio di due liquidi, uno a bassa densità e uno ad alta densità. Un'idea che lascia un po' scettico José Teixeira. E suggerisce che il responsabile sia ancora una volta il legame idrogeno. Ma come decidere, mentre la terra di nessuno rimane inaccessibile alle misurazioni? Una soluzione: migliorare gli esperimenti detti di cavitazione, che si svolgono a temperatura ambiente e a pressioni definite "negative".
Per José Teixeira, una conoscenza più approfondita della dinamica del legame idrogeno è indispensabile se si vuole davvero capire un giorno l'acqua. Bernard Cabane va anch'egli in questa direzione: « Ci mancano ancora molte informazioni sull'acqua per avere un modello realistico e predittivo del suo comportamento. Anche se conosciamo la natura dei legami tra molecole, finché non sapremo come una molecola isolata interagisce non solo con le prime vicine ma anche con le altre, il modello non sarà buono.» E le attuali simulazioni numeriche gli danno ragione. Infatti, se si cerca di spiegare le tre principali anomalie particolari dell'acqua, i modelli ne riproducono solo una o due. Mai tutte e tre contemporaneamente. Legame idrogeno: si stabilisce tra due molecole uguali o diverse. È il difetto di carica portato dall'atomo di idrogeno che permette l'apparizione del legame. Ma i fisici non mancano di idee per tentare di sciogliere il mistero. Per questo studiano la sua struttura a freddo. « I legami idrogeno sono più stabili al di sotto dei 0 °C», spiega José Teixeira. Si può quindi cercare di capire meglio l'acqua liquida seguendone l'evoluzione fino a -40 °C. Liquida fino a -40 °C? Sì, se è privata di tutte le impurità, altrimenti si cristallizza immediatamente. I ricercatori chiamano questo fenomeno la
superficie
(vedi diagramma di fase), che esiste anche per altri liquidi, come il toluene, il gallio o il silicio fuso. « Al momento, il record per l'acqua è a -42 °C – appena meglio dell'acqua surriscaldata presente in alcuni nuvole atmosferiche», precisa Frédéric Caupin, ricercatore al Laboratorio di Fisica Statistica dell'ENS. Al di sotto dei -40 °C, basta l'agitazione termica delle molecole d'acqua perché il liquido si trasformi in ghiaccio. Superata questa barriera di temperatura, la durata di vita dell'acqua liquida diventa estremamente breve. I fisici non hanno più modo di osservarla.

| E | lle
| mettono alla prova la coesione dell'acqua cercando la massima trazione che si può esercitare con ultrasuoni sull'acqua liquida prima che si formi la prima bollicina di vapore. « L'obiettivo è raggiungere una pressione di -1400 bar», commenta Frédéric Caupin. Allora avremmo nuovi elementi per escludere alcune ipotesi sulla struttura dell'acqua. Purtroppo, questi esperimenti sono oggi molto difficili da realizzare. Restano ancora progressi da compiere nella purificazione dell'acqua. Quindi pazienza. Il mistero dell'acqua rischia di tormentare i ricercatori per molti anni ancora, dice Julien Bourdet. Per sciogliere i misteri dell'acqua, i fisici contano sugli esperimenti di cavitazione (qui realizzati in un tunnel idrodinamico) dove appaiono bolle di vapore d'acqua. |
|---|
Tra le anomalie dell'acqua, le tre principali sono
-
una coesione molto forte, che si traduce in temperature di fusione e di ebollizione elevate;
-
una costante dielettrica elevata, che le permette di sciogliere tutti i sali.
Per sciogliere il mistero dell'acqua, i fisici contano sugli esperimenti di cavitazione (qui realizzati in un tunnel idrodinamico) dove appaiono bolle di vapore d'acqua
- una grande espansione a basse temperature (al di sotto dei 4 °C) e anche durante la cristallizzazione.
Così come si può trovare acqua surriscaldata, si può trovare anche surriscaldata, cioè liquida sopra i 100 °C. L'apparizione esplosiva di una bollicina si chiama cavitazione. Una caduta di pressione equivale a un riscaldamento dell'acqua. I ricercatori allungano l'acqua (parlano di pressione negativa) fino a osservare la prima bollicina di vapore.
Julien Bourdet
CONTATTI
Bemard Cabane: bcabane @ pmmh.espci.fr Frédéric Caupin: caupin @ lps.ens.fr José Teixeira: teix@ Ilb.saclay.ceafr

Tra le anomalie dell'acqua, le tre principali sono
-
una coesione molto forte, che si traduce in temperature di fusione e di ebollizione elevate;
-
una costante dielettrica elevata, che le permette di sciogliere tutti i sali.
Per sciogliere il mistero dell'acqua, i fisici contano sugli esperimenti di cavitazione (qui realizzati in un tunnel idrodinamico) dove appaiono bolle di vapore d'acqua
Tra le anomalie dell'acqua, le tre principali sono
-
una coesione molto forte, che si traduce in temperature di fusione e di ebollizione elevate;
-
una costante dielettrica elevata, che le permette di sciogliere tutti i sali.
Per sciogliere il mistero dell'acqua, i fisici contano sugli esperimenti di cavitazione (qui realizzati in un tunnel idrodinamico) dove appaiono bolle di vapore d'acqua
Verso "Opinione del CNRS sui lavori di Jean-Pierre Petit"
Ritorno al Guida Ritorno alla pagina principale
Numero di visite di questa pagina dal 8 marzo 2005: