mening van het CNRS over de werk van Jacques Benveniste
Zes maanden na zijn overlijden, de mening van het CNRS over de werk van J. Benveniste
8 maart 2005
Inleiding:



**
[De geluidsbestand van de interview met Montagnier, mei 2010](../../AUDIOS/LE SEPT NEUF DU DIMANCHE 02.05.2010_benveniste.mp3)
10 mei 2010.
Een lezer stuurde mij een fragment van een uitzending waarin de Nobelprijswinnaar Luc Montagnier de lof zingt over mijn verleden vriend Jacques Benveniste.
Professor Luc Montagnier, Nobelprijswinnaar voor geneeskunde, in 2007, te Lugano, hij spreekt niet om de hete brij en durft te verkondigen dat Jacques een geniale pionier was, vooruit op zijn tijd, en zijn overtuiging dat ooit de juistheid van zijn visie erkend zou worden.
Ik herinner me de tijd waarin de directeur van het INSERM, Lazare, Jacques zijn 200 vierkante meter lokalen bij het INSERM 200 in Clamart had afgenomen, wat hem ertoe bracht om zich opnieuw in de Algeco-barakken in de binnenplaats te installeren. Een absoluut schandaal.
Veel keer had ik Jacques gezegd "geef op, je zult je leven verliezen!" Maar hij hield vol, vasthield, tot zijn laatste adem, tot hij zijn leven verloor, met een verscheurd hart.
Mijn carrière had ook vergelijkbare aspecten en ik heb mijn leven gered omdat het slechts een ononderbroken reeks van opgegeven dingen was: MHD in 1972 (door het opgeven van de installatie die ik in 1967 had gebracht naar het internationaal voortrekkende laboratorium aan het Instituut voor Vloeimechanica in Marseille), informatica in 1983 (ik was onderdirecteur van het informatieservice van de universiteit van Provence), onderwijs in de faculteit voor letteren, wiskunde (de omkeer van de bol, Pour la Science 1979), een terugkeer naar MHD (1975-1986), opgeven van het uitgeven van stripboeken bij een uitgever in 1990, snelle opgave in de jaren duizend, in egyptologie. Momenteel, bijna opgegeven of serieus stilgelegd in astrofysica, kosmologie en wiskundige fysica, door gebrek aan positieve reacties (1985-2008).
Momenteel, een herstel met Savoir sans Frontières en heruitgave van boeken en stripverhalen. Activiteiten op de grens van opgeven in MHD en OVNIs. Hieronder de foto van de MHD-bank in montage in Rochefort (toestand in mei 2010) :
Dit is in de stijl van de Algeco's van Jacques, in de binnenplaats van het INSERM, met het verschil dat ik het niet zelf doe, maar een moedige technicus van 40 jaar. In tegenstelling tot Bernard Palissy, zul ik mijn meubels niet verbranden.
De Franse top MHD, de "niet in evenwicht" MHD, de "twee-temperatuur plasma's", die ons in staat stelt om op de eerste plaats te staan in internationale congressen (Vilnius 2008, Bremen 2009), daar is het!
Het zou grappig zijn als het niet zo triest was
Op de dag van het jaar van de fysica publiceerde het tijdschrift Le Courrier du CNRS een brochure met tien onopgeloste problemen in de wetenschap. Een van deze vragen betreft de structuur van water, in alle zijn vormen. Hieronder de afbeelding van deze dossier.

 | Tot nu toe zijn de fysici in staat geweest om te observeren dat ze voortdurend worden gecreëerd en vernietigd - elk leeft gemiddeld een duizendste van een biljardste seconde, dat er veel van hen worden gevormd en dat de drie betrokken atomen perfect uitgelijnd moeten zijn voor een binding te verschijnen. Nu, van alle vloeistoffen, is water de enige die deze drie kenmerken heeft. En waarschijnlijk is dit de reden waarom de beroemde anomaalies beschreven door de onderzoekers: aan de ene kant is water geen gas bij kamertemperatuur, omdat de waterstofbindingen sterk genoeg zijn. Water heeft dus een grote cohesiekracht. Resultaat: veel energie moet worden gegeven om deze bindingen te verbreken, wat verklaart dat het pas kookt bij 100 °C. Aan de andere kant is het ook geen vaste stof bij kamertemperatuur, omdat de bindingen toch kwetsbaar zijn. |
| Tot nu toe zijn de fysici in staat geweest om te observeren dat ze voortdurend worden gecreëerd en vernietigd - elk leeft gemiddeld een duizendste van een biljardste seconde, dat er veel van hen worden gevormd en dat de drie betrokken atomen perfect uitgelijnd moeten zijn voor een binding te verschijnen. Nu, van alle vloeistoffen, is water de enige die deze drie kenmerken heeft. En waarschijnlijk is dit de reden waarom de beroemde anomaalies beschreven door de onderzoekers: aan de ene kant is water geen gas bij kamertemperatuur, omdat de waterstofbindingen sterk genoeg zijn. Water heeft dus een grote cohesiekracht. Resultaat: veel energie moet worden gegeven om deze bindingen te verbreken, wat verklaart dat het pas kookt bij 100 °C. Aan de andere kant is het ook geen vaste stof bij kamertemperatuur, omdat de bindingen toch kwetsbaar zijn. |
|---|
** | P | our
| P | our
| José Teixeira is een dieper inzicht in de dynamiek van de waterstofbinding onmisbaar als we ooit echt willen begrijpen wat water is. Bernard Cabane gaat ook in die richting: "We hebben nog veel informatie nodig over water om een realistisch en voorspelbaar model van zijn gedrag te hebben. We weten de aard van de bindingen tussen moleculen, maar zolang we niet weten hoe een afzonderlijk molecuul zowel met zijn directe buren als met andere moleculen interageert, zal het model niet goed zijn. En de huidige numerieke simulaties geven hem gelijk. Inderdaad, als we de drie belangrijkste unieke eigenschappen van water willen verklaren, reproduceren de modellen slechts één of twee ervan. Nooit alle drie tegelijk. Waterstofbinding: deze ontstaat tussen twee identieke of niet-identieke moleculen. Het tekort aan lading op het waterstofatoom maakt de binding mogelijk. Maar de fysici hebben geen gebrek aan ideeën om het mysterie op te lossen. Daarom bestuderen ze zijn structuur bij koude temperaturen. "De waterstofbindingen zijn stabiler onder 0 °C", zegt José Teixeira. Dan kunnen we proberen het vloeibare water beter te begrijpen als we zijn evolutie volgen tot -40 °C. "Vloeibaar tot -40 °C? Ja, als het alle verontreinigingen is ontdaan, anders kristalliseert het direct. Wetenschappers noemen dit supergekoeld (zie fase-diagram), wat ook geldt voor andere vloeistoffen, zoals toluene, gallium of gesmolten silicium. "Tot nu toe is het record voor water op -42 °C - nauwelijks beter dan voor supergekoeld water in bepaalde atmosferische wolken, zegt Frédéric Caupin, onderzoeker aan het Laboratorium voor statistische fysica van de ENS. Onder -40 °C lijkt alleen de thermische beweging van watermoleculen voldoende om de vloeistof in ijs te veranderen. Boven die temperatuurbegrenzing wordt de levensduur van vloeibaar water extreem kort. Fysici hebben dan geen middel meer om het te observeren. |
|---|
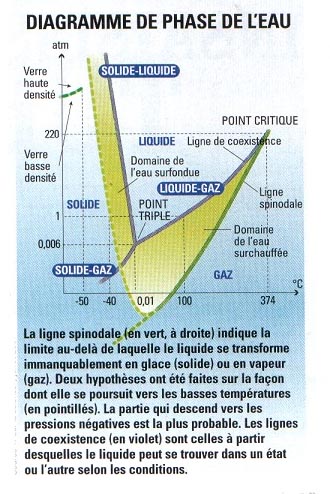
Het verschijnsel dat interessant is verschijnt rond -130 °C: als water voldoende snel wordt gekoeld tot deze temperatuur, verandert het in amorf ijs, dat wil zeggen dat het de structuur van glas heeft (zie p. 16). Een vaststelling: "We weten niets over de structuur van water tussen -40 °C en -130 °C", erkent José Teixeira. Met een beetje humor noemen de onderzoekers deze regio het "no man's land". Een wending in 1984: fysici Mishima, Calvert en Whalley ontdekten een tweede vorm van amorf ijs, dichter dan de eerste, door gewoon ijs op zeer lage temperaturen te comprimeren. Een resultaat dat oude ideeën weer opnieuw deed opkomen. Inderdaad, in 1892 had Röntgen de hypothese uitgesproken dat water een mengsel van vloeistof en ijs was. Vandaag zien sommigen in de ontdekking van de twee vormen van amorf ijs een belovende aanpak: water zou, ten minste bij lage temperaturen, een mengsel zijn van twee vloeistoffen, één met lage dichtheid en één met hoge dichtheid. Een idee dat José Teixeira een beetje sceptisch maakt. En hij suggereert dat het verantwoordelijke weer de waterstofbinding is. Maar hoe te beslissen, terwijl het "no man's land" nog steeds onbereikbaar is voor metingen? Een oplossing: verbeter de experimenten genaamd cavitation, die plaatsvinden bij kamertemperatuur en bij drukken die "negatief" worden genoemd.
voor José Teixeira is een dieper inzicht in de dynamiek van de waterstofbinding onmisbaar als we ooit echt willen begrijpen wat water is. Bernard Cabane gaat ook in die richting: "We hebben nog veel informatie nodig over water om een realistisch en voorspelbaar model van zijn gedrag te hebben. We weten de aard van de bindingen tussen moleculen, maar zolang we niet weten hoe een afzonderlijk molecuul zowel met zijn directe buren als met andere moleculen interageert, zal het model niet goed zijn. En de huidige numerieke simulaties geven hem gelijk. Inderdaad, als we de drie belangrijkste unieke eigenschappen van water willen verklaren, reproduceren de modellen slechts één of twee ervan. Nooit alle drie tegelijk. Waterstofbinding: deze ontstaat tussen twee identieke of niet-identieke moleculen. Het tekort aan lading op het waterstofatoom maakt de binding mogelijk. Maar de fysici hebben geen gebrek aan ideeën om het mysterie op te lossen. Daarom bestuderen ze zijn structuur bij koude temperaturen. "De waterstofbindingen zijn stabiler onder 0 °C", zegt José Teixeira. Dan kunnen we proberen het vloeibare water beter te begrijpen als we zijn evolutie volgen tot -40 °C. "Vloeibaar tot -40 °C? Ja, als het alle verontreinigingen is ontdaan, anders kristalliseert het direct. Wetenschappers noemen dit supergekoeld (zie fase-diagram), wat ook geldt voor andere vloeistoffen, zoals toluene, gallium of gesmolten silicium. "Tot nu toe is het record voor water op -42 °C - nauwelijks beter dan voor supergekoeld water in bepaalde atmosferische wolken, zegt Frédéric Caupin, onderzoeker aan het Laboratorium voor statistische fysica van de ENS. Onder -40 °C lijkt alleen de thermische beweging van watermoleculen voldoende om de vloeistof in ijs te veranderen. Boven die temperatuurbegrenzing wordt de levensduur van vloeibaar water extreem kort. Fysici hebben dan geen middel meer om het te observeren.
voor José Teixeira is een dieper inzicht in de dynamiek van de waterstofbinding onmisbaar als we ooit echt willen begrijpen wat water is. Bernard Cabane gaat ook in die richting: "We hebben nog veel informatie nodig over water om een realistisch en voorspelbaar model van zijn gedrag te hebben. We weten de aard van de bindingen tussen moleculen, maar zolang we niet weten hoe een afzonderlijk molecuul zowel met zijn directe buren als met andere moleculen interageert, zal het model niet goed zijn. En de huidige numerieke simulaties geven hem gelijk. Inderdaad, als we de drie belangrijkste unieke eigenschappen van water willen verklaren, reproduceren de modellen slechts één of twee ervan. Nooit alle drie tegelijk. Waterstofbinding: deze ontstaat tussen twee identieke of niet-identieke moleculen. Het tekort aan lading op het waterstofatoom maakt de binding mogelijk. Maar de fysici hebben geen gebrek aan ideeën om het mysterie op te lossen. Daarom bestuderen ze zijn structuur bij koude temperaturen. "De waterstofbindingen zijn stabiler onder 0 °C", zegt José Teixeira. Dan kunnen we proberen het vloeibare water beter te begrijpen als we zijn evolutie volgen tot -40 °C. "Vloeibaar tot -40 °C? Ja, als het alle verontreinigingen is ontdaan, anders kristalliseert het direct. Wetenschappers noemen dit supergekoeld (zie fase-diagram), wat ook geldt voor andere vloeistoffen, zoals toluene, gallium of gesmolten silicium. "Tot nu toe is het record voor water op -42 °C - nauwelijks beter dan voor supergekoeld water in bepaalde atmosferische wolken, zegt Frédéric Caupin, onderzoeker aan het Laboratorium voor statistische fysica van de ENS. Onder -40 °C lijkt alleen de thermische beweging van watermoleculen voldoende om de vloeistof in ijs te veranderen. Boven die temperatuurbegrenzing wordt de levensduur van vloeibaar water extreem kort. Fysici hebben dan geen middel meer om het te observeren.

| E | lles
| testen de cohesie van water door de maximale trekkracht te zoeken die je kunt uitoefenen met ultrasone golven op vloeibaar water voordat de eerste dampbel verschijnt. "Het doel is om een druk van -1400 bar te bereiken", zegt Frédéric Caupin. "Dan zouden we nieuwe elementen krijgen die bepaalde hypothese over de structuur van water zouden kunnen uitsluiten." Helaas zijn deze experimenten momenteel erg moeilijk uit te voeren. Er zijn nog vooruitgangen nodig in de reiniging van water. Dus geduld. Het mysterie van water zal waarschijnlijk de onderzoekers nog jaren bezig houden, zegt Julien Bourdet. Om de mysteries van water op te lossen, vertrouwen fysici op cavitatie-experimenten (hier uitgevoerd in een hydrodynamische windtunnel) waarin waterdampbelletjes verschijnen. |
|---|
Onder de anomaalies van water zijn de drie belangrijkste
-
een zeer sterke cohesie, wat leidt tot hoge smelt- en kookpunten;
-
een hoge diëlectrische constante, die het mogelijk maakt om alle zouten op te lossen.
Om het mysterie van water op te lossen, vertrouwen fysici op cavitatie-experimenten (hier uitgevoerd in een hydrodynamische windtunnel) waarin waterdampbelletjes verschijnen
- een grote uitbreiding bij lage temperaturen (onder 4 °C) en ook tijdens de kristallisatie.
Zoals je supergekoeld water kunt vinden, kun je ook oververhit water vinden, dat wil zeggen vloeibaar boven 100 °C. Het explosieve verschijnen van een bel wordt cavitatie genoemd. Een drukdaling is gelijk aan verwarmen van water. De onderzoekers trekken het water (ze spreken van negatieve druk) tot ze de eerste dampbel waarnemen.
**Julien Bourdet **
CONTACTS
Bemard Cabane : bcabane @ pmmh.espci.fr Frédéric Caupin : caupin @ lps.ens.fr José Teixeira : teix@ Ilb.saclay.ceafr

Onder de anomaalies van water zijn de drie belangrijkste
-
een zeer sterke cohesie, wat leidt tot hoge smelt- en kookpunten;
-
een hoge diëlectrische constante, die het mogelijk maakt om alle zouten op te lossen.
Om het mysterie van water op te lossen, vertrouwen fysici op cavitatie-experimenten (hier uitgevoerd in een hydrodynamische windtunnel) waarin waterdampbelletjes verschijnen
Onder de anomaalies van water zijn de drie belangrijkste
-
een zeer sterke cohesie, wat leidt tot hoge smelt- en kookpunten;
-
een hoge diëlectrische constante, die het mogelijk maakt om alle zouten op te lossen.
Om het mysterie van water op te lossen, vertrouwen fysici op cavitatie-experimenten (hier uitgevoerd in een hydrodynamische windtunnel) waarin waterdampbelletjes verschijnen
Vers " Menin van het CNRS over de werk van Jean-Pierre Petit "
Retour naar Gids Retour naar de startpagina
Aantal keer dat deze pagina is bekeken sinds 8 maart 2005 :