opinião do CNRS sobre os trabalhos de Jacques Benveniste
Seis meses após sua morte, a opinião do CNRS sobre os trabalhos de J. Benveniste
8 de março de 2005
Em preliminar:



**
[O arquivo de áudio da entrevista com Montagnier, maio de 2010](../../AUDIOS/LE SEPT NEUF DU DIMANCHE 02.05.2010_benveniste.mp3)
10 de maio de 2010.
Um leitor me enviou um trecho de uma emissão em que se ouve o prêmio Nobel Luc Montagnier elogiando meu querido amigo falecido Jacques Benveniste.
O professor Luc Montagnier, prêmio Nobel de Medicina em 2007, em Lugano, não se contém e não hesita em declarar que Jacques foi um precursor genial, à frente de seu tempo, e sua convicção de que um dia se reconheceria a correção de suas ideias.
Lembro-me da época em que o diretor geral do INSERM, Lazare, retirou de Jacques seus 200 metros quadrados de espaço no INSERM 200 de Clamart, o que o levou a se reinstalar nos barracos Algeco, no pátio! Uma verdadeira vergonha.
Muitas vezes disse a Jacques: "desista, você vai acabar morrendo por isso!". Mas ele se agarrou, se agarrou até o último suspiro, até deixar sua vida, o coração dilacerado.
Minha carreira apresentou aspectos semelhantes e só sobrevivi porque foi uma sucessão ininterrupta de abandonos: MHD em 1972 (abandonando no Instituto de Mecânica dos Fluidos de Marselha o equipamento com o qual havia trazido em 1967 o laboratório à vanguarda internacional), Informática em 1983 (era subdiretor do serviço de informática da Universidade de Provence), ensino na faculdade de letras e matemáticas (reversão da esfera, Pour la Science 1979), uma volta à MHD (1975-1986), abandono da edição de quadrinhos com um editor, em 1990, abandono rápido, nos anos 2000, em egiptologia. Atualmente, quase abandono ou suspensão séria em astrofísica, cosmologia e física matemática, por falta de respostas positivas (1985-2008).
Atualmente, renovação com Savoir sans Frontières e reedição de livros e quadrinhos. Atividades quase abandonadas em MHD e tema OVNIs. Abaixo, a foto do banco MHD em montagem em Rochefort (estado em maio de 2010):
É no estilo dos Algeco de Jacques, no pátio do INSERM, com a diferença de que não sou eu quem se ocupa disso, mas um corajoso técnico de 40 anos. Ao contrário de Bernard Palissy, eu não queimarei meus móveis.
A MHD francesa de ponta, a MHD "fora do equilíbrio", a dos "plasmas bitemperatura", que nos permite figurar na liderança em congressos internacionais (Vilnius 2008, Bremen 2009), aqui está!
Seria cômico se não fosse de uma tristeza absoluta.
Em ocasião do Ano da Física, a revista Le Courrier du CNRS publicou um folheto apresentando dez problemas não resolvidos na ciência. Uma dessas questões concerne à estrutura da água em todos os seus estados. Abaixo, reprodução desse dossier.

 | Até o momento, os físicos conseguiram observar que elas se criam e se destroem continuamente — cada uma vive em média um milésimo de milionésimo de segundo, que um grande número delas se forma e que é necessário que os três átomos envolvidos estejam perfeitamente alinhados para que uma ligação surja. Ora, entre todos os líquidos, a água é o único que reúne essas três características. E é provavelmente isso que explica, em parte, as famosas anomalias descritas pelos pesquisadores: de um lado, a água não é um gás à temperatura ambiente, porque as ligações de hidrogênio são suficientemente fortes. A água, portanto, possui uma grande força de coesão. Resultado: é necessário fornecer muita energia para romper essas ligações, o que explica por que ela só ferve a 100 °C. De outro lado, tampouco é um sólido à temperatura ambiente, porque as ligações são ainda frágeis.
| Até o momento, os físicos conseguiram observar que elas se criam e se destroem continuamente — cada uma vive em média um milésimo de milionésimo de segundo, que um grande número delas se forma e que é necessário que os três átomos envolvidos estejam perfeitamente alinhados para que uma ligação surja. Ora, entre todos os líquidos, a água é o único que reúne essas três características. E é provavelmente isso que explica, em parte, as famosas anomalias descritas pelos pesquisadores: de um lado, a água não é um gás à temperatura ambiente, porque as ligações de hidrogênio são suficientemente fortes. A água, portanto, possui uma grande força de coesão. Resultado: é necessário fornecer muita energia para romper essas ligações, o que explica por que ela só ferve a 100 °C. De outro lado, tampouco é um sólido à temperatura ambiente, porque as ligações são ainda frágeis.
|---|
** | P | ara
| P | ara
| José Teixeira, um conhecimento mais profundo da dinâmica da ligação de hidrogênio é indispensável se quisermos realmente compreender a água algum dia. Bernard Cabane também vai nesse sentido: "Ainda nos faltam muitas informações sobre a água para termos um modelo realista e preditivo de seu comportamento. Sabemos a natureza das ligações entre moléculas, mas enquanto não soubermos como uma molécula isolada interage não apenas com suas vizinhas imediatas, mas também com as demais, o modelo não será bom". E as simulações numéricas atuais dão razão a ele. De fato, se tentamos explicar as três principais anomalias particulares da água, os modelos reproduzem apenas uma ou duas. Nunca as três ao mesmo tempo. Ligação de hidrogênio: estabelece-se entre duas moléculas iguais ou não. É o déficit de carga do átomo de hidrogênio que permite a formação da ligação. Mas os físicos não estão sem ideias para tentar desvendar o mistério. Para isso, estudam sua estrutura em frio. "As ligações de hidrogênio são mais estáveis abaixo de 0 °C", explica José Teixeira. Assim, podemos tentar compreender melhor a água líquida seguindo sua evolução até -40 °C." Líquida até -40 °C? Sim, se estiver livre de todas as impurezas, caso contrário cristaliza imediatamente. Os cientistas chamam isso de superaquecimento (ver diagrama de fase), que também existe para outros líquidos, como o tolueno, o gálio ou a sílica fundida. "Atualmente, o recorde para a água é de -42 °C — apenas um pouco melhor que a água superaquecida presente em certas nuvens atmosféricas", afirma Frédéric Caupin, pesquisador no Laboratório de Física Estatística da ENS. Abaixo de -40 °C, basta a agitação térmica das moléculas de água para que o líquido se transforme em gelo. Após essa barreira de temperatura, a vida útil da água líquida torna-se extremamente curta. Os físicos então não têm mais como observá-la. |
|---|
É em torno de -130 °C que surge outro fenômeno interessante: se a água for resfriada suficientemente rápido até essa temperatura, transforma-se em gelo amorfo, ou seja, tem a estrutura do vidro (ver p. 16). Uma constatação se impõe: "Não sabemos nada sobre a estrutura da água entre -40 °C e -130 °C", admite José Teixeira. Sem perder o humor, os pesquisadores chamam essa zona de "terra de ninguém". Reviravolta em 1984: os físicos Mishima, Calvert e Whalley descobrem uma segunda forma de gelo amorfo, mais densa que a primeira, comprimindo o gelo comum a temperaturas muito baixas. Um resultado que ressuscitou ideias antigas. De fato, em 1892, Röntgen havia proposto a hipótese de que a água era uma mistura de líquido e gelo. Hoje, alguns veem na descoberta das duas formas de gelo amorfo uma pista promissora: a água seria, pelo menos em baixas temperaturas, uma mistura de dois líquidos, um de baixa densidade e outro de alta densidade. Uma ideia que deixa um pouco cético José Teixeira. E ele sugere que o responsável ainda é, sempre, a ligação de hidrogênio. Mas como decidir, enquanto a "terra de ninguém" permanece inacessível às medições? Uma solução: melhorar as experiências chamadas de cavitação, que ocorrem à temperatura ambiente e sob pressões qualificadas de "negativas".
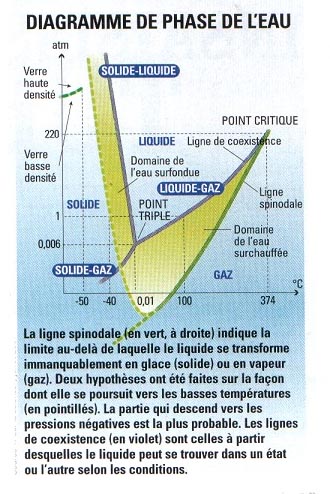
Para José Teixeira, um conhecimento mais profundo da dinâmica da ligação de hidrogênio é indispensável se quisermos realmente compreender a água algum dia. Bernard Cabane também vai nesse sentido: "Ainda nos faltam muitas informações sobre a água para termos um modelo realista e preditivo de seu comportamento. Sabemos a natureza das ligações entre moléculas, mas enquanto não soubermos como uma molécula isolada interage não apenas com suas vizinhas imediatas, mas também com as demais, o modelo não será bom". E as simulações numéricas atuais dão razão a ele. De fato, se tentamos explicar as três principais anomalias particulares da água, os modelos reproduzem apenas uma ou duas. Nunca as três ao mesmo tempo. Ligação de hidrogênio: estabelece-se entre duas moléculas iguais ou não. É o déficit de carga do átomo de hidrogênio que permite a formação da ligação. Mas os físicos não estão sem ideias para tentar desvendar o mistério. Para isso, estudam sua estrutura em frio. "As ligações de hidrogênio são mais estáveis abaixo de 0 °C", explica José Teixeira. Assim, podemos tentar compreender melhor a água líquida seguindo sua evolução até -40 °C." Líquida até -40 °C? Sim, se estiver livre de todas as impurezas, caso contrário cristaliza imediatamente. Os cientistas chamam isso de superaquecimento (ver diagrama de fase), que também existe para outros líquidos, como o tolueno, o gálio ou a sílica fundida. "Atualmente, o recorde para a água é de -42 °C — apenas um pouco melhor que a água superaquecida presente em certas nuvens atmosféricas", afirma Frédéric Caupin, pesquisador no Laboratório de Física Estatística da ENS. Abaixo de -40 °C, basta a agitação térmica das moléculas de água para que o líquido se transforme em gelo. Após essa barreira de temperatura, a vida útil da água líquida torna-se extremamente curta. Os físicos então não têm mais como observá-la.
Para José Teixeira, um conhecimento mais profundo da dinâmica da ligação de hidrogênio é indispensável se quisermos realmente compreender a água algum dia. Bernard Cabane também vai nesse sentido: "Ainda nos faltam muitas informações sobre a água para termos um modelo realista e preditivo de seu comportamento. Sabemos a natureza das ligações entre moléculas, mas enquanto não soubermos como uma molécula isolada interage não apenas com suas vizinhas imediatas, mas também com as demais, o modelo não será bom". E as simulações numéricas atuais dão razão a ele. De fato, se tentamos explicar as três principais anomalias particulares da água, os modelos reproduzem apenas uma ou duas. Nunca as três ao mesmo tempo. Ligação de hidrogênio: estabelece-se entre duas moléculas iguais ou não. É o déficit de carga do átomo de hidrogênio que permite a formação da ligação. Mas os físicos não estão sem ideias para tentar desvendar o mistério. Para isso, estudam sua estrutura em frio. "As ligações de hidrogênio são mais estáveis abaixo de 0 °C", explica José Teixeira. Assim, podemos tentar compreender melhor a água líquida seguindo sua evolução até -40 °C." Líquida até -40 °C? Sim, se estiver livre de todas as impurezas, caso contrário cristaliza imediatamente. Os cientistas chamam isso de superaquecimento (ver diagrama de fase), que também existe para outros líquidos, como o tolueno, o gálio ou a sílica fundida. "Atualmente, o recorde para a água é de -42 °C — apenas um pouco melhor que a água superaquecida presente em certas nuvens atmosféricas", afirma Frédéric Caupin, pesquisador no Laboratório de Física Estatística da ENS. Abaixo de -40 °C, basta a agitação térmica das moléculas de água para que o líquido se transforme em gelo. Após essa barreira de temperatura, a vida útil da água líquida torna-se extremamente curta. Os físicos então não têm mais como observá-la.

| E | l
| as testam a coesão da água procurando a tração máxima que pode ser exercida com ultrassons sobre a água líquida antes que a primeira bolha de vapor se forme. "A esperança é alcançar uma pressão de -1400 barras", comenta Frédéric Caupin. "Assim, teríamos novos elementos que permitiriam descartar algumas hipóteses sobre a estrutura da água." Infelizmente, essas experiências são hoje muito difíceis de realizar. Ainda há progressos a serem feitos na purificação da água. Paciência, portanto. O mistério da água provavelmente continuará perturbando os pesquisadores por muitos anos, diz Julien Bourdet. Para desvendar os mistérios da água, os físicos contam com experiências de cavitação (aqui realizadas em um túnel hidrodinâmico) onde aparecem bolhas de vapor d'água. |
|---|
Entre as anomalias da água, as três principais são
-
uma coesão muito forte, que se traduz por temperaturas de fusão e ebulição elevadas;
-
uma constante dielétrica elevada, que lhe permite dissolver todos os sais.
Para desvendar o mistério da água, os físicos contam com experiências de cavitação (aqui realizadas em um túnel hidrodinâmico) onde aparecem bolhas de vapor d'água.
- uma grande expansão em baixas temperaturas (abaixo de 4 °C) e também durante a cristalização.
Assim como se pode encontrar água superaquecida, também se pode encontrar superaquecida, ou seja, líquida acima de 100 °C. A formação explosiva de uma bolha chama-se cavitação. Uma queda de pressão equivale a um aquecimento da água. Os pesquisadores esticam a água (falam em pressão negativa) até observar a primeira bolha de vapor.
Julien Bourdet
CONTATOS
Bernard Cabane: bcabane @ pmmh.espci.fr Frédéric Caupin: caupin @ lps.ens.fr José Teixeira: teix@ Ilb.saclay.ceafr

Entre as anomalias da água, as três principais são
-
uma coesão muito forte, que se traduz por temperaturas de fusão e ebulição elevadas;
-
uma constante dielétrica elevada, que lhe permite dissolver todos os sais.
Para desvendar o mistério da água, os físicos contam com experiências de cavitação (aqui realizadas em um túnel hidrodinâmico) onde aparecem bolhas de vapor d'água.
Entre as anomalias da água, as três principais são
-
uma coesão muito forte, que se traduz por temperaturas de fusão e ebulição elevadas;
-
uma constante dielétrica elevada, que lhe permite dissolver todos os sais.
Para desvendar o mistério da água, os físicos contam com experiências de cavitação (aqui realizadas em um túnel hidrodinâmico) onde aparecem bolhas de vapor d'água.
Voltar para "Opinião do CNRS sobre os trabalhos de Jean-Pierre Petit"
Retornar ao Guia Retornar à página inicial
Número de visualizações desta página desde 8 de março de 2005: