opinia CNRS privind lucrările lui Jacques Benveniste
Şase luni după decesul său, opinia CNRS privind lucrările lui J. Benveniste
8 martie 2005
În prefață:



**
[Fișierul audio al interviului cu Montagnier, mai 2010](../../AUDIOS/LE SEPT NEUF DU DIMANCHE 02.05.2010_benveniste.mp3)
10 mai 2010.
Un cititor mi-a trimis un fragment dintr-o emisiune în care se aude premiul Nobel Luc Montagnier lăudând pe prietenul meu decedat, Jacques Benveniste.
Profesorul Luc Montagnier, laureat al Premiului Nobel pentru medicină în 2007, la Lugano, nu ezită să declare că Jacques a fost un precurgător genial, înainte de timpul său, și că el crede ferm că într-o zi se va recunoaște corectitudinea viziunilor sale.
Îmi amintesc perioada în care directorul general al INSERM, Lazare, i-a retras lui Jacques cei 200 de metri pătrați de spațiu de la INSERM 200 din Clamart, ceea ce l-a obligat să se refacă în barăci Algeco, în curte! O adevărată jignire.
De multe ori i-am spus lui Jacques: „Renunță, o să-ți pui viața în pericol!”. Dar el s-a agățat, s-a agățat, până la ultima suflare, până ce și-a lăsat viața acolo, cu inima ruptă.
Cariera mea a avut aspecte similare și nu îmi datorez supraviețuirea decât faptului că a fost doar o succesiune neîntreruptă de renunțări: MHD în 1972 (renunțând la instalația cu care am adus în 1967 laboratorul la nivel internațional), informatică în 1983 (erau subdirector al serviciului de informatică al Universității din Provence), predare în facultatea de litere, matematici (întoarcerea sferei, Pour la Science 1979), un comeback în MHD (1975-1986), renunțarea la editarea BD-urilor la un editor, în 1990, renunțare rapidă în anii 2000 în egiptologie. În prezent, aproape abandon sau o punere serioasă în repaus în astrofizică, cosmologie și fizică matematică, din cauza lipsei de răspuns pozitiv (1985-2008).
În prezent, un nou început cu Savoir sans Frontières și reeditarea cărților și a BD-urilor. Activități la limita abandonului în MHD și subiectul OVNIs. Mai jos, fotografia băncii MHD în curs de montare la Rochefort (stare în mai 2010):
Este stilul barăcilor Algeco ale lui Jacques, în curtea INSERM, cu diferența că nu eu mă ocup de aceasta, ci un tehnician curajos de 40 de ani. În contrast cu Bernard Palissy, eu nu voi arde mobilierul.
MHD franceză de vârf, MHD „din afara echilibrului”, cea a „plasmei bitemperaturale”, care ne permite să fim printre primii în conferințe internaționale (Vilnius 2008, Bremen 2009), iată-o!
Ar fi comic dacă nu ar fi o tristețe absolută.
În cadrul Anului Fizicii, revista Le Courrier du CNRS a publicat o broșură prezentând zece probleme nerezolvate în știință. Una dintre aceste întrebări se referă la structura apei, în toate stările sale. Mai jos, reproducerea dosarului.

 | Până în prezent, fizicienii au reușit să observe că se creează și se distrug fără încetare – fiecare trăiește în medie un miliardime de milionime de secundă, că un număr mare dintre ele se formează și că trei atomi trebuie să fie perfect aliniați pentru ca o legătură să apară. Din toate lichidele, apa este singura care reuneste aceste trei caracteristici. Și probabil acest lucru explică în parte cele cunoscute anomalii descrise de cercetători: pe de o parte, apa nu este un gaz la temperatura camerei, pentru că legăturile hidrogenului sunt suficient de puternice. Apa are deci o mare forță de coeziune. Rezultatul: trebuie să adăugăm multă energie pentru a rupe aceste legături, ceea ce explică de ce nu fierbe decât la 100 °C. Pe de altă parte, nu este nici solid la temperatura camerei, pentru că legăturile sunt totuși fragile. |
| Până în prezent, fizicienii au reușit să observe că se creează și se distrug fără încetare – fiecare trăiește în medie un miliardime de milionime de secundă, că un număr mare dintre ele se formează și că trei atomi trebuie să fie perfect aliniați pentru ca o legătură să apară. Din toate lichidele, apa este singura care reuneste aceste trei caracteristici. Și probabil acest lucru explică în parte cele cunoscute anomalii descrise de cercetători: pe de o parte, apa nu este un gaz la temperatura camerei, pentru că legăturile hidrogenului sunt suficient de puternice. Apa are deci o mare forță de coeziune. Rezultatul: trebuie să adăugăm multă energie pentru a rupe aceste legături, ceea ce explică de ce nu fierbe decât la 100 °C. Pe de altă parte, nu este nici solid la temperatura camerei, pentru că legăturile sunt totuși fragile. |
|---|
** | P | entru
| P | entru
| José Teixeira, o cunoaștere mai profundă a dinamicii legăturii hidrogenului este esențială dacă vrem să înțelegem vreodată apa. Bernard Cabane merge și el în aceeași direcție: „Încă ne lipsesc multe informații despre apă pentru a avea un model realist și predictiv al comportamentului ei. Chiar dacă cunoaștem natura legăturilor dintre molecule, atâta timp cât nu vom ști cum o moleculă izolată interacționează nu doar cu vecinii săi imediat, ci și cu ceilalți, modelul nu va fi bun. Iar simulările numerice actuale îi dau dreptate. Într-adevăr, dacă încercăm să explicăm cele trei principale anomalii specifice ale apei, modelele reușesc să reproducă doar una sau două dintre ele. Niciodată toate trei în același timp. Legătura hidrogenului: se stabilește între două molecule identice sau nu. Deficitul de sarcină pe care îl are atomul de hidrogen permite apariția legăturii. Dar fizicienii nu sunt lipsiți de idei pentru a încerca să dezvăluie misterul. Pentru aceasta, ei studiază structura sa la rece. „Legăturile hidrogenului sunt mai stabile sub 0 °C”, explică José Teixeira. Putem atunci încerca să înțelegem mai bine apa lichidă dacă urmărim evoluția ei până la -40 °C.” Lichidă până la -40 °C? Da, dacă este curățată de toate impuritățile, altfel cristalizează imediat. Cercetătorii numesc acest lucru suprafuziune (vedeți diagrama de fază), care există și pentru alte lichide, cum ar fi toluenul, galiumul sau silicea topită. „Până în prezent, recordul pentru apă este la -42 °C – doar puțin mai bine decât apa suprafuzată din anumite nori atmosferici”, precizează Frédéric Caupin, cercetător la Laboratorul de fizică statistică al ENS. Sub -40 °C, chiar agitația termică a moleculelor de apă pare suficientă pentru ca lichidul să se transforme în gheață. Odată depășită această barieră de temperatură, durata de viață a apei lichide devine extrem de scurtă. Fizicienii nu mai au mijloacele de a o observa. |
|---|
Este în jurul temperaturii de -130 °C că apare un alt fenomen interesant: dacă apa este răcită suficient de repede până la această temperatură, se transformă în gheață amorfa, adică are structura sticlei (vedeți pagina 16). O constatare se impune: „Nu știm nimic despre structura apei între -40 °C și -130 °C”, recunoaște José Teixeira. Fără să fie serios, cercetătorii numesc această zonă „ținutul nimeni nu e”. O întoarcere în 1984: fizicienii Mishima, Calvert și Whalley descoperă o a doua formă de gheață, amorfa, mai densă decât prima, comprimând gheața obișnuită la temperaturi foarte joase. Un rezultat care a readus în discuție vechi ipoteze. Într-adevăr, în 1892, Röntgen a emis ipoteza că apa ar fi un amestec de lichid și gheață. Astăzi, unii văd în descoperirea celor două forme de gheață amorfe o pistă promițătoare: apa ar fi, cel puțin la temperaturi joase, un amestec de două lichide, unul cu densitate mică și altul cu densitate mare. O idee care lasă puțin sceptic pe José Teixeira. Și el sugerează că responsabilul este din nou legătura hidrogenului. Dar cum se poate decide, dacă „ținutul nimeni nu e” rămâne inaccesibil măsurătorilor? O soluție: a îmbunătăți experimentele de cavitație, care se desfășoară la temperatura camerei și la presiuni numite „negative”.
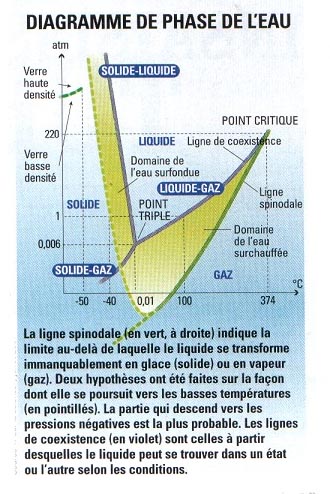
Pentru José Teixeira, o cunoaștere mai profundă a dinamicii legăturii hidrogenului este esențială dacă vrem să înțelegem vreodată apa. Bernard Cabane merge și el în aceeași direcție: „Încă ne lipsesc multe informații despre apă pentru a avea un model realist și predictiv al comportamentului ei. Chiar dacă cunoaștem natura legăturilor dintre molecule, atâta timp cât nu vom ști cum o moleculă izolată interacționează nu doar cu vecinii săi imediat, ci și cu ceilalți, modelul nu va fi bun. Iar simulările numerice actuale îi dau dreptate. Într-adevăr, dacă încercăm să explicăm cele trei principale anomalii specifice ale apei, modelele reușesc să reproducă doar una sau două dintre ele. Niciodată toate trei în același timp. Legătura hidrogenului: se stabilește între două molecule identice sau nu. Deficitul de sarcină pe care îl are atomul de hidrogen permite apariția legăturii. Dar fizicienii nu sunt lipsiți de idei pentru a încerca să dezvăluie misterul. Pentru aceasta, ei studiază structura sa la rece. „Legăturile hidrogenului sunt mai stabile sub 0 °C”, explică José Teixeira. Putem atunci încerca să înțelegem mai bine apa lichidă dacă urmărim evoluția ei până la -40 °C.” Lichidă până la -40 °C? Da, dacă este curățată de toate impuritățile, altfel cristalizează imediat. Cercetătorii numesc acest lucru suprafuziune (vedeți diagrama de fază), care există și pentru alte lichide, cum ar fi toluenul, galiumul sau silicea topită. „Până în prezent, recordul pentru apă este la -42 °C – doar puțin mai bine decât apa suprafuzată din anumite nori atmosferici”, precizează Frédéric Caupin, cercetător la Laboratorul de fizică statistică al ENS. Sub -40 °C, chiar agitația termică a moleculelor de apă pare suficientă pentru ca lichidul să se transforme în gheață. Odată depășită această barieră de temperatură, durata de viață a apei lichide devine extrem de scurtă. Fizicienii nu mai au mijloacele de a o observa.
Pentru José Teixeira, o cunoaștere mai profundă a dinamicii legăturii hidrogenului este esențială dacă vrem să înțelegem vreodată apa. Bernard Cabane merge și el în aceeași direcție: „Încă ne lipsesc multe informații despre apă pentru a avea un model realist și predictiv al comportamentului ei. Chiar dacă cunoaștem natura legăturilor dintre molecule, atâta timp cât nu vom ști cum o moleculă izolată interacționează nu doar cu vecinii săi imediat, ci și cu ceilalți, modelul nu va fi bun. Iar simulările numerice actuale îi dau dreptate. Într-adevăr, dacă încercăm să explicăm cele trei principale anomalii specifice ale apei, modelele reușesc să reproducă doar una sau două dintre ele. Niciodată toate trei în același timp. Legătura hidrogenului: se stabilește între două molecule identice sau nu. Deficitul de sarcină pe care îl are atomul de hidrogen permite apariția legăturii. Dar fizicienii nu sunt lipsiți de idei pentru a încerca să dezvăluie misterul. Pentru aceasta, ei studiază structura sa la rece. „Legăturile hidrogenului sunt mai stabile sub 0 °C”, explică José Teixeira. Putem atunci încerca să înțelegem mai bine apa lichidă dacă urmărim evoluția ei până la -40 °C.” Lichidă până la -40 °C? Da, dacă este curățată de toate impuritățile, altfel cristalizează imediat. Cercetătorii numesc acest lucru suprafuziune (vedeți diagrama de fază), care există și pentru alte lichide, cum ar fi toluenul, galiumul sau silicea topită. „Până în prezent, recordul pentru apă este la -42 °C – doar puțin mai bine decât apa suprafuzată din anumite nori atmosferici”, precizează Frédéric Caupin, cercetător la Laboratorul de fizică statistică al ENS. Sub -40 °C, chiar agitația termică a moleculelor de apă pare suficientă pentru ca lichidul să se transforme în gheață. Odată depășită această barieră de temperatură, durata de viață a apei lichide devine extrem de scurtă. Fizicienii nu mai au mijloacele de a o observa.

| E | le
| testă coeziunea apei căutând tracțiunea maximă pe care o putem exercita cu ultrasonori asupra apei lichide înainte ca prima bule de vapori să apară. „Speranța este să atingem o presiune de -1400 bar”, comentă Frédéric Caupin. Atunci, am avea elemente noi care ne-ar permite să eliminăm unele ipoteze despre structura apei.” Din păcate, aceste experimente sunt astăzi foarte dificil de realizat. Mai trebuie făcuți progrese în curățarea apei. Așadar, răbdare. MISTERUL APEI va deranja cercetătorii încă multe ani, spune Julien Bourdet. Pentru a dezvălui misterul apei, fizicienii se bazează pe experimentele de cavitație (aici realizate într-un tunel hidrodinamic) unde apar bule de vapori de apă. |
|---|
Printre anomaile apei, cele trei principale sunt
-
o coeziune foarte mare, care se traduce prin temperaturi ridicate de topire și fierbere;
-
o constantă dielectrică ridicată, care îi permite să dizolve toți sălții.
Pentru a dezvălui misterul apei, fizicienii se bazează pe experimentele de cavitație (aici realizate într-un tunel hidrodinamic) unde apar bule de vapori de apă
- o mare expansiune la temperaturi joase (sub 4 °C) și de asemenea în timpul cristalizării.
La fel cum putem găsi apă suprafuzată, putem găsi și apă supratemperată, adică lichidă peste 100 °C. Apariția explozivă a unei bule se numește cavitație. O scădere a presiunii este echivalentă cu încălzirea apei. Cercetătorii întind apa (vorbind despre presiune negativă) până observă prima bulă de vapori.
Julien Bourdet
CONTACTE
Bemard Cabane: bcabane @ pmmh.espci.fr Frédéric Caupin: caupin @ lps.ens.fr José Teixeira: teix@ Ilb.saclay.ceafr

Printre anomaile apei, cele trei principale sunt
-
o coeziune foarte mare, care se traduce prin temperaturi ridicate de topire și fierbere;
-
o constantă dielectrică ridicată, care îi permite să dizolve toți sălții.
Pentru a dezvălui misterul apei, fizicienii se bazează pe experimentele de cavitație (aici realizate într-un tunel hidrodinamic) unde apar bule de vapori de apă
Printre anomaile apei, cele trei principale sunt
-
o coeziune foarte mare, care se traduce prin temperaturi ridicate de topire și fierbere;
-
o constantă dielectrică ridicată, care îi permite să dizolve toți sălții.
Pentru a dezvălui misterul apei, fizicienii se bazează pe experimentele de cavitație (aici realizate într-un tunel hidrodinamic) unde apar bule de vapori de apă
Versus " Opinia CNRS privind lucrările lui Jean-Pierre Petit "
Înapoi la ghid Înapoi la pagina principală
Numărul de vizualizări ale acestei pagini de la 8 martie 2005: