Meinung des CNRS zu den Arbeiten von Jacques Benveniste
Sechs Monate nach seinem Tod: Meinung des CNRS zu den Arbeiten von J. Benveniste
- März 2005
Vorwort:



**
[Das Tonfile des Interviews mit Montagnier, Mai 2010](../../AUDIOS/LE SEPT NEUF DU DIMANCHE 02.05.2010_benveniste.mp3)
- Mai 2010.
Ein Leser hat mir Ausschnitte einer Sendung geschickt, in der man den Nobelpreisträger Luc Montagnier lobt, der meinen verstorbenen Freund Jacques Benveniste bewundert.
Professor Luc Montagnier, Nobelpreisträger für Medizin, 2007, in Lugano, er sagt ohne Umschweife, dass Jacques ein genialer Vorreiter war, der seiner Zeit voraus war, und er ist überzeugt, dass eines Tages die Richtigkeit seiner Ansichten anerkannt werden wird.
Ich erinnere mich an die Zeit, als der Generalsekretär des INSERM, Lazare, Jacques seine 200 Quadratmeter großen Räume im INSERM 200 in Clamart weggenommen hat, was dazu führte, dass er in den Baracken Algeco in den Hof umziehen musste. Eine absolute Schande.
Ich habe Jacques oft gesagt: "Gib auf, du wirst dein Leben verlieren!" Doch er hielt fest, fest, bis zu seinem letzten Atemzug, bis er sein Leben verlor, mit einem zerrissenen Herzen.
Meine Karriere hatte ähnliche Aspekte, und ich verdanke mein Leben nur, weil sie eine ununterbrochene Kette von Aufgaben war: MHD 1972 (bei dem ich 1967 das Labor, das international führend war, dem Institut für Fluiddynamik in Marseille übertragen hatte), Informatik 1983 (ich war stellvertretender Leiter des Informati-onsdienstes der Universität von Provence), Unterricht an der Fakultät für Literatur und Mathematik (Kugelumdrehung, Pour la Science 1979), ein Comeback in der MHD (1975-1986), Verlagsabandon in der BD 1990, schnelles Abandon in den 2000er Jahren in der Ägyptologie. Derzeit fast Abandon oder ernsthafte Pause in Astrophysik, Kosmologie und mathematischer Physik, aufgrund fehlender positiver Reaktionen (1985-2008).
Derzeit gibt es einen Neuanfang mit "Savoir sans Frontières" und der Neuausgabe von Büchern und BD. Grenzabandon in der MHD und OVNI-Themen. Hier die Fotos des MHD-Bänks im Aufbau in Rochefort (Stand Mai 2010):
Es ist in dem Stil der Algeco-Baracken von Jacques, im Hof des INSERM, mit dem Unterschied, dass ich es nicht selbst betreue, sondern ein mutiger Techniker im Alter von 40 Jahren. Im Unterschied zu Bernard Palissy werde ich meine Möbel nicht verbrennen.
Die führende französische MHD, die "nicht im Gleichgewicht" stehende MHD, jene der "zweitemperatur-Plasmen", die uns in internationalen Konferenzen in der ersten Reihe platziert (Vilnius 2008, Bremen 2009), das ist sie!
Es wäre komisch, wenn es nicht so traurig wäre
Anlässlich des Jahres der Physik hat die Zeitschrift Le Courrier du CNRS eine Broschüre veröffentlicht, die zehn ungelöste Probleme in der Wissenschaft vorstellt. Eine dieser Fragen betrifft die Struktur des Wassers in allen seinen Zuständen. Hier ist die Wiedergabe dieses Dossiers.

 | Bis jetzt haben die Physiker es geschafft, zu beobachten, dass sie ständig entstehen und verschwinden - jede lebt im Durchschnitt ein Milliardstel Sekunde, viele von ihnen entstehen und es ist erforderlich, dass die drei beteiligten Atome perfekt ausgerichtet sind, damit eine Verbindung entsteht. Nun, von allen Flüssigkeiten ist Wasser die einzige, die diese drei Merkmale besitzt. Und das erklärt vermutlich teilweise die berühmten Anomalien, die von den Forschern beschrieben wurden: auf der einen Seite ist Wasser bei Raumtemperatur kein Gas, weil die Wasserstoffbrückenbindungen stark genug sind. Wasser hat also eine große Kohäsionskraft. Ergebnis: Es ist notwendig, viel Energie aufzuwenden, um diese Bindungen zu brechen, was erklärt, warum es erst bei 100 °C kocht. Auf der anderen Seite ist es jedoch auch kein Feststoff bei Raumtemperatur, weil die Bindungen dennoch zerbrechlich sind. |
| Bis jetzt haben die Physiker es geschafft, zu beobachten, dass sie ständig entstehen und verschwinden - jede lebt im Durchschnitt ein Milliardstel Sekunde, viele von ihnen entstehen und es ist erforderlich, dass die drei beteiligten Atome perfekt ausgerichtet sind, damit eine Verbindung entsteht. Nun, von allen Flüssigkeiten ist Wasser die einzige, die diese drei Merkmale besitzt. Und das erklärt vermutlich teilweise die berühmten Anomalien, die von den Forschern beschrieben wurden: auf der einen Seite ist Wasser bei Raumtemperatur kein Gas, weil die Wasserstoffbrückenbindungen stark genug sind. Wasser hat also eine große Kohäsionskraft. Ergebnis: Es ist notwendig, viel Energie aufzuwenden, um diese Bindungen zu brechen, was erklärt, warum es erst bei 100 °C kocht. Auf der anderen Seite ist es jedoch auch kein Feststoff bei Raumtemperatur, weil die Bindungen dennoch zerbrechlich sind. |
|---|
** | P | our
| P | our
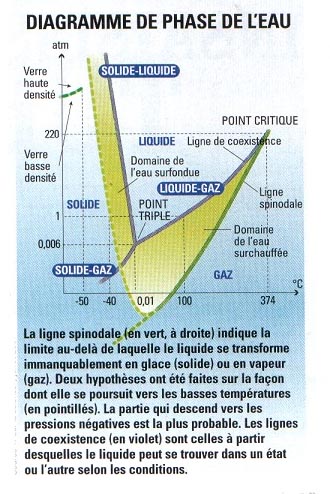
| José Teixeira ist eine tiefere Kenntnis der Dynamik der Wasserstoffbrückenbindung unerlässlich, wenn man Wasser eines Tages wirklich verstehen will. Bernard Cabane geht in dieselbe Richtung: „Wir fehlen noch viele Informationen über Wasser, um ein realistisches und vorhersagbares Modell seines Verhaltens zu haben. Obwohl wir die Natur der Bindungen zwischen Molekülen kennen, wird das Modell nicht gut sein, solange wir nicht wissen, wie ein einzelnes Molekül nicht nur mit seinen nächsten Nachbarn, sondern auch mit anderen interagiert. „Und die aktuellen numerischen Simulationen haben ihm Recht gegeben. Tatsächlich, wenn man versucht, die drei wichtigsten besonderen Anomalien des Wassers zu erklären, reproduzieren die Modelle nur eine oder zwei davon. Nie alle drei gleichzeitig. Wasserstoffbrücke: Sie bildet sich zwischen zwei gleichen oder unterschiedlichen Molekülen. Es ist der Ladungsmangel des Wasserstoffatoms, der die Bildung der Bindung ermöglicht. Doch die Physiker haben nicht die geringste Idee, um das Geheimnis zu lüften. Dazu untersuchen sie seine Struktur bei Kälte. „Die Wasserstoffbrückenbindungen sind unter 0 °C stabiler“, erklärt José Teixeira. „Man kann dann versuchen, das flüssige Wasser besser zu verstehen, wenn man seine Entwicklung bis zu -40 °C verfolgt.“ Flüssig bis -40 °C? Ja, wenn es alle seine Verunreinigungen losgeworden ist, andernfalls kristallisiert es sofort. Die Wissenschaftler nennen das „Überkühlung“ (siehe Phasendiagramm), was auch für andere Flüssigkeiten wie Toluol, Gallium oder geschmolzenes Silizium gilt. „Derzeit ist der Rekord für Wasser bei -42 °C - kaum besser als für das überkühlte Wasser in bestimmten atmosphärischen Wolken“, sagt Frédéric Caupin, Forscher am Laboratoire de physique statistique de l’ENS. Unter -40 °C scheint nur die thermische Bewegung der Wassermoleküle auszureichen, um das flüssige Wasser in Eis zu verwandeln. Sobald diese Temperaturschwelle überschritten ist, wird die Lebensdauer des flüssigen Wassers extrem kurz. Die Physiker haben dann keine Möglichkeit mehr, es zu beobachten. |
|---|
Es ist in der Nähe von -130 °C, dass ein weiteres interessantes Phänomen auftritt: Wenn Wasser schnell genug gekühlt wird, bis zu dieser Temperatur, verwandelt es sich in amorphes Eis, das heißt, es hat die Struktur von Glas (siehe S. 16). Eine Beobachtung ergibt sich: „Wir wissen nichts über die Struktur des Wassers zwischen -40 °C und -130 °C“, gibt José Teixeira zu. Ohne Humor nennen die Forscher diese Zone das „kein Land“. Eine Wendung 1984: Die Physiker Mishima, Calvert und Whalley entdeckten eine zweite Form von amorphem Eis, dichter als die erste, indem sie normales Eis bei sehr niedriger Temperatur komprimierten. Ein Ergebnis, das alte Ideen wiederbelebte. Tatsächlich hatte Röntgen 1892 die Hypothese aufgestellt, dass Wasser ein Gemisch aus Flüssigkeit und Eis sei. Heute sehen einige in der Entdeckung der beiden Formen von amorphem Eis eine vielversprechende Spur: Wasser wäre zumindest bei niedrigen Temperaturen ein Gemisch aus zwei Flüssigkeiten, einer mit niedriger Dichte und einer mit hoher Dichte. Eine Idee, die José Teixeira etwas skeptisch macht. Und er schlägt vor, dass der Verantwortliche immer noch die Wasserstoffbrückenbindung sei. Doch wie soll man entscheiden, wenn das „kein Land“ weiterhin unzugänglich für Messungen bleibt? Eine Lösung: Verbesserung der sogenannten Kavitationsversuche, die bei Raumtemperatur und unter sogenannten „negativen“ Drücken stattfinden.
für José Teixeira ist eine tiefere Kenntnis der Dynamik der Wasserstoffbrückenbindung unerlässlich, wenn man Wasser eines Tages wirklich verstehen will. Bernard Cabane geht in dieselbe Richtung: „Wir fehlen noch viele Informationen über Wasser, um ein realistisches und vorhersagbares Modell seines Verhaltens zu haben. Obwohl wir die Natur der Bindungen zwischen Molekülen kennen, wird das Modell nicht gut sein, solange wir nicht wissen, wie ein einzelnes Molekül nicht nur mit seinen nächsten Nachbarn, sondern auch mit anderen interagiert. „Und die aktuellen numerischen Simulationen haben ihm Recht gegeben. Tatsächlich, wenn man versucht, die drei wichtigsten besonderen Anomalien des Wassers zu erklären, reproduzieren die Modelle nur eine oder zwei davon. Nie alle drei gleichzeitig. Wasserstoffbrücke: Sie bildet sich zwischen zwei gleichen oder unterschiedlichen Molekülen. Es ist der Ladungsmangel des Wasserstoffatoms, der die Bildung der Bindung ermöglicht. Doch die Physiker haben nicht die geringste Idee, um das Geheimnis zu lüften. Dazu untersuchen sie seine Struktur bei Kälte. „Die Wasserstoffbrückenbindungen sind unter 0 °C stabiler“, erklärt José Teixeira. „Man kann dann versuchen, das flüssige Wasser besser zu verstehen, wenn man seine Entwicklung bis zu -40 °C verfolgt.“ Flüssig bis -40 °C? Ja, wenn es alle seine Verunreinigungen losgeworden ist, andernfalls kristallisiert es sofort. Die Wissenschaftler nennen das „Überkühlung“ (siehe Phasendiagramm), was auch für andere Flüssigkeiten wie Toluol, Gallium oder geschmolzenes Silizium gilt. „Derzeit ist der Rekord für Wasser bei -42 °C - kaum besser als für das überkühlte Wasser in bestimmten atmosphärischen Wolken“, sagt Frédéric Caupin, Forscher am Laboratoire de physique statistique de l’ENS. Unter -40 °C scheint nur die thermische Bewegung der Wassermoleküle auszureichen, um das flüssige Wasser in Eis zu verwandeln. Sobald diese Temperaturschwelle überschritten ist, wird die Lebensdauer des flüssigen Wassers extrem kurz. Die Physiker haben dann keine Möglichkeit mehr, es zu beobachten.
für José Teixeira ist eine tiefere Kenntnis der Dynamik der Wasserstoffbrückenbindung unerlässlich, wenn man Wasser eines Tages wirklich verstehen will. Bernard Cabane geht in dieselbe Richtung: „Wir fehlen noch viele Informationen über Wasser, um ein realistisches und vorhersagbares Modell seines Verhaltens zu haben. Obwohl wir die Natur der Bindungen zwischen Molekülen kennen, wird das Modell nicht gut sein, solange wir nicht wissen, wie ein einzelnes Molekül nicht nur mit seinen nächsten Nachbarn, sondern auch mit anderen interagiert. „Und die aktuellen numerischen Simulationen haben ihm Recht gegeben. Tatsächlich, wenn man versucht, die drei wichtigsten besonderen Anomalien des Wassers zu erklären, reproduzieren die Modelle nur eine oder zwei davon. Nie alle drei gleichzeitig. Wasserstoffbrücke: Sie bildet sich zwischen zwei gleichen oder unterschiedlichen Molekülen. Es ist der Ladungsmangel des Wasserstoffatoms, der die Bildung der Bindung ermöglicht. Doch die Physiker haben nicht die geringste Idee, um das Geheimnis zu lüften. Dazu untersuchen sie seine Struktur bei Kälte. „Die Wasserstoffbrückenbindungen sind unter 0 °C stabiler“, erklärt José Teixeira. „Man kann dann versuchen, das flüssige Wasser besser zu verstehen, wenn man seine Entwicklung bis zu -40 °C verfolgt.“ Flüssig bis -40 °C? Ja, wenn es alle seine Verunreinigungen losgeworden ist, andernfalls kristallisiert es sofort. Die Wissenschaftler nennen das „Überkühlung“ (siehe Phasendiagramm), was auch für andere Flüssigkeiten wie Toluol, Gallium oder geschmolzenes Silizium gilt. „Derzeit ist der Rekord für Wasser bei -42 °C - kaum besser als für das überkühlte Wasser in bestimmten atmosphärischen Wolken“, sagt Frédéric Caupin, Forscher am Laboratoire de physique statistique de l’ENS. Unter -40 °C scheint nur die thermische Bewegung der Wassermoleküle auszureichen, um das flüssige Wasser in Eis zu verwandeln. Sobald diese Temperaturschwelle überschritten ist, wird die Lebensdauer des flüssigen Wassers extrem kurz. Die Physiker haben dann keine Möglichkeit mehr, es zu beobachten.

| E | lles
| prüfen die Kohäsion des Wassers, indem sie die maximale Zugkraft suchen, die man mit Ultraschall auf flüssiges Wasser ausüben kann, bevor die erste Dampfblase entsteht. „Die Hoffnung ist, eine Druck von -1400 Bar zu erreichen“, kommentiert Frédéric Caupin. „Dann hätten wir neue Elemente, die es ermöglichen, bestimmte Hypothesen über die Struktur des Wassers zu ausschließen.“ Leider sind diese Experimente heute sehr schwierig durchzuführen. Noch Fortschritte sind in der Reinigung des Wassers erforderlich. Geduld also. Das Geheimnis des Wassers wird die Forscher noch viele Jahre beschäftigen, sagt Julien Bourdet. Um die Geheimnisse des Wassers zu lüften, setzen Physiker auf Kavitationsexperimente (hier in einem hydrodynamischen Tunnel durchgeführt), bei denen Dampfblasen auftreten. |
|---|
Zu den Anomalien des Wassers gehören drei Hauptanomalien:
-
eine sehr starke Kohäsion, die sich in hohen Schmelz- und Siedepunkten zeigt;
-
eine hohe dielektrische Konstante, die es ermöglicht, alle Salze zu lösen.
Um das Geheimnis des Wassers zu lüften, setzen Physiker auf Kavitationsexperimente (hier in einem hydrodynamischen Tunnel durchgeführt), bei denen Dampfblasen auftreten
- eine große Ausdehnung bei niedrigen Temperaturen (unter 4 °C) und auch bei der Kristallisation.
Ebenso wie man überkühltes Wasser finden kann, kann man auch überhitztes Wasser finden, also flüssig über 100 °C. Die explosionsartige Bildung einer Blase wird Kavitation genannt. Ein Druckabfall entspricht einem Erwärmen des Wassers. Die Forscher dehnen das Wasser (sie sprechen von negativem Druck) bis sie die erste Dampfblase beobachten.
**Julien Bourdet **
KONTAKTE
Bemard Cabane : bcabane @ pmmh.espci.fr Frédéric Caupin : caupin @ lps.ens.fr José Teixeira : teix@ Ilb.saclay.ceafr

Zu den Anomalien des Wassers gehören drei Hauptanomalien:
-
eine sehr starke Kohäsion, die sich in hohen Schmelz- und Siedepunkten zeigt;
-
eine hohe dielektrische Konstante, die es ermöglicht, alle Salze zu lösen.
Um das Geheimnis des Wassers zu lüften, setzen Physiker auf Kavitationsexperimente (hier in einem hydrodynamischen Tunnel durchgeführt), bei denen Dampfblasen auftreten
Zu den Anomalien des Wassers gehören drei Hauptanomalien:
-
eine sehr starke Kohäsion, die sich in hohen Schmelz- und Siedepunkten zeigt;
-
eine hohe dielektrische Konstante, die es ermöglicht, alle Salze zu lösen.
Um das Geheimnis des Wassers zu lüften, setzen Physiker auf Kavitationsexperimente (hier in einem hydrodynamischen Tunnel durchgeführt), bei denen Dampfblasen auftreten
Vers " Meinung des CNRS zu den Arbeiten von Jean-Pierre Petit "
Zurück zum Leitfaden Zurück zur Startseite
Anzahl der Besuche dieser Seite seit dem 8. März 2005 :