opinión del CNRS sobre los trabajos de Jacques Benveniste
Seis meses después de su fallecimiento, la opinión del CNRS sobre los trabajos de J. Benveniste
8 de marzo de 2005
En preámbulo:



**
[El archivo de audio de la entrevista a Montagnier, mayo de 2010](../../AUDIOS/LE SEPT NEUF DU DIMANCHE 02.05.2010_benveniste.mp3)
10 de mayo de 2010.
Un lector me envió un fragmento de un programa en el que se escucha al premio Nobel Luc Montagnier elogiando a mi querido amigo Jacques Benveniste.
El profesor Luc Montagnier, galardonado con el Premio Nobel de Medicina en 2007 en Lugano, no se anda con rodeos y no duda en declarar que Jacques fue un precursor genial, adelantado a su tiempo, y que está convencido de que algún día se reconocerá la validez de sus ideas.
Recuerdo la época en que el director general del INSERM, Lazare, le retiró a Jacques sus 200 metros cuadrados de instalaciones en el INSERM 200 de Clamart, lo que lo obligó a reubicarse en unas cabañas Algeco, en el patio. Una verdadera vergüenza.
Muchas veces le dije a Jacques: "abandona, vas a dejar tu vida allí". Pero se aferró, se aferró hasta su último aliento, hasta que dejó su vida, con el corazón destrozado.
Mi carrera también ha tenido aspectos similares y solo he salvado la vida porque ha sido una sucesión ininterrumpida de abandonos: MHD en 1972 (al abandonar en el Instituto de Mecánica de Fluidos de Marsella el equipo con el que había llevado en 1967 el laboratorio a la vanguardia internacional), informática en 1983 (era subdirector del servicio de informática de la Universidad de Provenza), enseñanza en facultad de letras y matemáticas (inversión de la esfera, Pour la Science 1979), un regreso a la MHD (1975-1986), abandono de edición de cómics con una editorial en 1990, abandono rápido en los años 2000 en egiptología. Actualmente, casi abandono o serio apagón en astrofísica, cosmología y física matemática, por falta de respuestas positivas (1985-2008).
Actualmente, un nuevo impulso con Savoir sans Frontières y reedición de libros y cómics. Actividades al borde del abandono en MHD y temas OVNIs. A continuación, la foto del banco MHD en proceso de montaje en Rochefort (estado en mayo de 2010):
Es en el estilo de las cabañas Algeco de Jacques, en el patio del INSERM, a diferencia de que ahora no soy yo quien se ocupa, sino un valiente técnico de 40 años. A diferencia de Bernard Palissy, no quemaré mis muebles.
¡La MHD francesa de vanguardia, la MHD "fuera de equilibrio", la de los "plasmas bitemperatura", que nos permite figurar entre los primeros en congresos internacionales (Vilnius 2008, Bremen 2009), ¡ahí está!
Sería cómico si no fuera una tristeza absoluta.
En ocasión del Año de la Física, la revista Le Courrier du CNRS publicó una hoja informativa presentando diez problemas sin resolver en ciencia. Una de estas preguntas concierne a la estructura del agua en todos sus estados. A continuación, reproducimos dicho dossier.

 | Por ahora, los físicos han logrado observar que se crean y destruyen continuamente —cada una dura en promedio una milésima de milbillonésima de segundo—, que un gran número de ellas se forman y que es necesario que los tres átomos implicados estén perfectamente alineados para que aparezca un enlace. Sin embargo, entre todos los líquidos, el agua es el único que reúne estas tres características. Y probablemente sea esto lo que explique en parte las famosas anomalías descritas por los investigadores: por un lado, el agua no es un gas a temperatura ambiente, porque los enlaces de hidrógeno son lo suficientemente fuertes. Por tanto, el agua posee una gran fuerza de cohesión. Resultado: se necesita mucha energía para romper estos enlaces, lo que explica que hierva solo a 100 °C. Por otro lado, tampoco es un sólido a temperatura ambiente, porque los enlaces son aún frágiles. |
| Por ahora, los físicos han logrado observar que se crean y destruyen continuamente —cada una dura en promedio una milésima de milbillonésima de segundo—, que un gran número de ellas se forman y que es necesario que los tres átomos implicados estén perfectamente alineados para que aparezca un enlace. Sin embargo, entre todos los líquidos, el agua es el único que reúne estas tres características. Y probablemente sea esto lo que explique en parte las famosas anomalías descritas por los investigadores: por un lado, el agua no es un gas a temperatura ambiente, porque los enlaces de hidrógeno son lo suficientemente fuertes. Por tanto, el agua posee una gran fuerza de cohesión. Resultado: se necesita mucha energía para romper estos enlaces, lo que explica que hierva solo a 100 °C. Por otro lado, tampoco es un sólido a temperatura ambiente, porque los enlaces son aún frágiles. |
|---|
** | P | ara
| P | ara
| José Teixeira, una comprensión más profunda de la dinámica del enlace de hidrógeno es indispensable si queremos realmente entender el agua algún día. Bernard Cabane también va en esa dirección: « Nos falta aún mucha información sobre el agua para tener un modelo realista y predictivo de su comportamiento. Aunque conozcamos la naturaleza de los enlaces entre moléculas, mientras no sepamos cómo una molécula aislada interactúa no solo con sus primeros vecinos, sino también con las demás, el modelo no será bueno.» Y las simulaciones numéricas actuales le dan la razón. De hecho, si intentamos explicar las tres principales anomalías particulares del agua, los modelos solo reproducen una o dos. Nunca las tres a la vez. Enlace de hidrógeno: se establece entre dos moléculas iguales o no. Es la deficiencia de carga del átomo de hidrógeno la que permite la aparición del enlace. Pero los físicos no carecen de ideas para intentar resolver el misterio. Para ello, estudian su estructura a baja temperatura. « Los enlaces de hidrógeno son más estables por debajo de 0 °C», explica José Teixeira. Entonces, podemos intentar comprender mejor el agua líquida si seguimos su evolución hasta los -40 °C. ¿Líquida hasta los -40 °C? Sí, si se deshace de todas sus impurezas; de lo contrario, cristaliza inmediatamente. Los científicos llaman a esto la sobreenfriamiento (ver diagrama de fases), que también existe para otros líquidos, como el tolueno, el galio o la sílice fundida. « Por ahora, el récord para el agua está en -42 °C —ligeramente mejor que el agua sobreenfriada presente en algunas nubes atmosféricas», precisa Frédéric Caupin, investigador del Laboratorio de Física Estadística de la ENS. Por debajo de -40 °C, simplemente la agitación térmica de las moléculas de agua parece suficiente para que el líquido se transforme en hielo. Una vez superada esta barrera de temperatura, la vida útil del agua líquida se vuelve extremadamente breve. Los físicos ya no tienen forma de observarla. |
|---|
Es alrededor de los -130 °C cuando aparece otro fenómeno interesante: si el agua se enfría lo suficientemente rápido hasta esta temperatura, se transforma en hielo amorfo, es decir, tiene la estructura del vidrio (ver p. 16). Una constatación se impone: « No sabemos nada sobre la estructura del agua entre -40 °C y -130 °C», reconoce José Teixeira. Sin falta de humor, los investigadores llaman a esta zona el «tierra de nadie». Giro inesperado en 1984: los físicos Mishima, Calvert y Whalley descubrieron una segunda forma de hielo amorfo, más densa que la primera, al comprimir el hielo ordinario a muy baja temperatura. Un hallazgo que ha resucitado ideas antiguas. En efecto, en 1892, Röntgen había propuesto la hipótesis de que el agua era una mezcla de líquido y hielo. Hoy en día, algunos ven en el descubrimiento de las dos formas de hielo amorfo una pista prometedora: el agua sería, al menos a bajas temperaturas, una mezcla de dos líquidos, uno de baja densidad y otro de alta densidad. Una idea que deja algo escéptico a José Teixeira. Y sugiere que el responsable sigue siendo, una vez más, el enlace de hidrógeno. Pero ¿cómo decidir, si la tierra de nadie sigue inaccesible a las mediciones? Una solución: mejorar las experiencias de cavitación, que se llevan a cabo a temperatura ambiente y a presiones calificadas de «negativas».
Para José Teixeira, una comprensión más profunda de la dinámica del enlace de hidrógeno es indispensable si queremos realmente entender el agua algún día. Bernard Cabane también va en esa dirección: « Nos falta aún mucha información sobre el agua para tener un modelo realista y predictivo de su comportamiento. Aunque conozcamos la naturaleza de los enlaces entre moléculas, mientras no sepamos cómo una molécula aislada interactúa no solo con sus primeros vecinos, sino también con las demás, el modelo no será bueno.» Y las simulaciones numéricas actuales le dan la razón. De hecho, si intentamos explicar las tres principales anomalías particulares del agua, los modelos solo reproducen una o dos. Nunca las tres a la vez. Enlace de hidrógeno: se establece entre dos moléculas iguales o no. Es la deficiencia de carga del átomo de hidrógeno la que permite la aparición del enlace. Pero los físicos no carecen de ideas para intentar resolver el misterio. Para ello, estudian su estructura a baja temperatura. « Los enlaces de hidrógeno son más estables por debajo de 0 °C», explica José Teixeira. Entonces, podemos intentar comprender mejor el agua líquida si seguimos su evolución hasta los -40 °C. ¿Líquida hasta los -40 °C? Sí, si se deshace de todas sus impurezas; de lo contrario, cristaliza inmediatamente. Los científicos llaman a esto la
sobreenfriamiento
(ver diagrama de fases), que también existe para otros líquidos, como el tolueno, el galio o la sílice fundida. « Por ahora, el récord para el agua está en -42 °C —ligeramente mejor que el agua sobreenfriada presente en algunas nubes atmosféricas», precisa Frédéric Caupin, investigador del Laboratorio de Física Estadística de la ENS. Por debajo de -40 °C, simplemente la agitación térmica de las moléculas de agua parece suficiente para que el líquido se transforme en hielo. Una vez superada esta barrera de temperatura, la vida útil del agua líquida se vuelve extremadamente breve. Los físicos ya no tienen forma de observarla.

| E | llas
| ponen a prueba la cohesión del agua buscando la tracción máxima que se puede ejercer con ultrasonidos sobre el agua líquida antes de que aparezca la primera burbuja de vapor. « La esperanza es alcanzar una presión de -1400 bares», comenta Frédéric Caupin. Entonces, tendríamos nuevos elementos que permitirían descartar ciertas hipótesis sobre la estructura del agua. Desafortunadamente, estas experiencias son hoy muy difíciles de realizar. Aún quedan progresos por hacer en la purificación del agua. Paciencia, pues. El misterio del agua probablemente seguirá inquietando a los investigadores durante muchas más años, dice Julien Bourdet. Para desentrañar los misterios del agua, los físicos apuestan por experiencias de cavitación (aquí realizadas en un túnel hidrodinámico) donde aparecen burbujas de vapor de agua. |
|---|
Entre las anomalías del agua, las tres principales son
-
una cohesión muy fuerte, que se traduce en temperaturas de fusión y ebullición elevadas;
-
una constante dieléctrica alta, que le permite disolver todos los sales.
Para desentrañar el misterio del agua, los físicos apuestan por experiencias de cavitación (aquí realizadas en un túnel hidrodinámico) donde aparecen burbujas de vapor de agua
- una gran expansión a bajas temperaturas (por debajo de 4 °C) y también durante la cristalización.
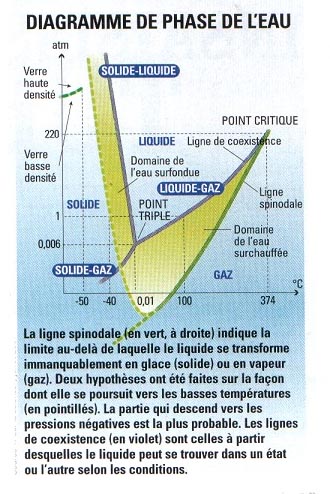
Al igual que se puede encontrar agua sobreenfriada, también se puede encontrar sobrecalentada, es decir, líquida por encima de 100 °C. La aparición explosiva de una burbuja se llama cavitación. Una caída de presión equivale a un calentamiento del agua. Los investigadores estiran el agua (hablan de presión negativa) hasta observar la primera burbuja de vapor.
Julien Bourdet
CONTACTOS
Bernard Cabane: bcabane @ pmmh.espci.fr Frédéric Caupin: caupin @ lps.ens.fr José Teixeira: teix@ Ilb.saclay.ceafr

Entre las anomalías del agua, las tres principales son
-
una cohesión muy fuerte, que se traduce en temperaturas de fusión y ebullición elevadas;
-
una constante dieléctrica alta, que le permite disolver todos los sales.
Para desentrañar el misterio del agua, los físicos apuestan por experiencias de cavitación (aquí realizadas en un túnel hidrodinámico) donde aparecen burbujas de vapor de agua
Entre las anomalías del agua, las tres principales son
-
una cohesión muy fuerte, que se traduce en temperaturas de fusión y ebullición elevadas;
-
una constante dieléctrica alta, que le permite disolver todos los sales.
Para desentrañar el misterio del agua, los físicos apuestan por experiencias de cavitación (aquí realizadas en un túnel hidrodinámico) donde aparecen burbujas de vapor de agua
Volver a "Opinión del CNRS sobre los trabajos de Jean-Pierre Petit"
Volver al Guía Volver a la página principal
Número de consultas de esta página desde el 8 de marzo de 2005: